设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.11.2 L N2所含分子数为0.5NA |
| B.常温下,16 g CH4中共用电子对的数目为4NA |
| C.一定温度下,1 mol FeCl3水解生成NA个Fe(OH)3胶体颗粒 |
| D.在反应H2O2+Cl2=2HCl+O2中,每生成32 g氧气,转移4NA个电子 |
ClO2是新一代饮用水的消毒剂,许多发达国家的自来水厂采用ClO2代替Cl2来进行自来水消毒。我国最近成功研制出制取ClO2的新方法,其反应的微观过程如下所示: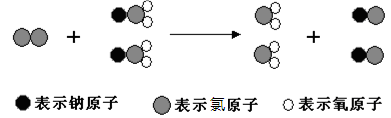
下列有关该反应的叙述中正确的是()
| A.该反应是复分解反应 |
| B.该反应的化学方程式为Cl2+2NaClO2====2ClO2+2NaCl |
| C.反应中Cl2既是氧化剂,又是还原剂 |
| D.NaClO2和ClO2中Cl的化合价相同 |
下列说法不正确的是()
| A.制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 |
| B.除去CO2气体中混有的少量SO2,可以将气体通入足量酸性KMnO4溶液中 |
| C.H2在Cl2中燃烧火焰呈淡蓝色 |
| D.在Cl2制备实验中,用饱和食盐水除去Cl2中的HCl气体,用NaOH溶液吸收尾气 |
保护环境,就是关爱自己。下列说法中你认为不正确的是()
| A.空气质量日报的主要目的是树立人们环保意识,同时也让人们知道了二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物 |
| B.酸雨是指pH小于7的雨水 |
| C.为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须回收处理 |
| D.居室污染是来自建筑、装饰和家具材料散发出的甲醛等有害气体 |
“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。下列化学反应符合“绿色化学”理念的是()
| A.制CuSO4:Cu + 2H2SO4(浓)= CuSO4 + SO2↑+ 2H2O |
| B.制CuSO4:2Cu + O2= 2CuO; Cu + H2SO4(稀)= CuSO4 + H2O |
| C.制Cu(NO3)2:Cu + 4HNO3(浓)= Cu(NO3)2 +2NO2↑+ 2H2O |
| D.制Cu(NO3)2:3Cu + 8HNO3(稀)= 3Cu(NO3)2 +2NO↑+ 4H2O |
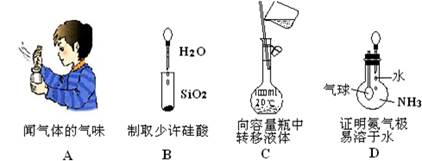
下列各图所示的实验操作,不能达到相应的实验目的的是()