将煤转化为水煤气的主要化学反应为C(s)+H2O(g) CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)=H2O(g) ΔH=-242.0 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学方程式:________。
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律作出下列循环图:
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。
请分析:甲、乙两同学观点正确的是________(填“甲”或“乙”);判断的理由是________。
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点________。
(4)水煤气不仅是优良的气体燃料,也是重要的有机化工原料。CO和H2在一定条件下可以合成:①甲醇;②甲醛;③甲酸;④乙酸。试分析当CO和H2按1:1的体积比混合反应,合成上述________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放。
(附加题)某气态烷烃和乙烯等体积混合时,1体积混合气体完全燃烧消耗同 温同压下4.75体积氧气。试回答:
温同压下4.75体积氧气。试回答:
(1)该烷烃的分子式为;
(2)该烷烃所有同分异构 体的结构简式为。
体的结构简式为。
已知乙烯能发生以下转化:
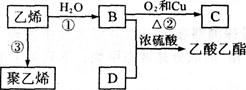
(1)乙烯的结构式为:_________________________。
(2)写出下列化合物官能团的名称:
B中含官能团名称___________;D中含官能团名称____________。
(3)写出反应的化学方程式及反应类型:
①______________________________________________;反应类型:________。
②_____________________________________________。
在2008 年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
 (1)该融雪剂的化学式是;Y的最高价氧化物的水化物中含有的化学键是。
(1)该融雪剂的化学式是;Y的最高价氧化物的水化物中含有的化学键是。 (2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为。
(2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为。 (3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。
(3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。 (4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为:
(4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为: _______________________ ______________________。
_______________________ ______________________。
(1)食物中的营养物质主要包括:糖类、_______、蛋白质、维生素、无机盐、__________。
(2)迄今为止,煤、石油、_____________仍是人类使用的主要能源,它们同属于化石能源,是不可再生能源,需要合理开发利用。
(3)淀粉在稀酸的催化作用下,能最终水解为葡萄糖,欲检验淀粉是否完全水解,可 以在水解反应混合物中滴加_______________溶液,通过溶液有没有发生显色反应来判断。
以在水解反应混合物中滴加_______________溶液,通过溶液有没有发生显色反应来判断。
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①它们的电子层数之和为10;②Z、W元素的原子最外层电子数之和是X元素原子最外层电子数的2倍;③Z和W元素原子质子数之和是X、Y元素原子质子数之和的2倍;④X元素的原子最外层电子数是次外层电子数的2倍。回答下列问题:
(1)X元素为__________,Y元素为____________;
(2)Z元素位于周期表的第________周期;
(3)过量X的最高价氧化物通入氢氧化钠溶液中,小心蒸干,得到固体为:___________;
(4)若Z为钠,则W为;XYW2的结构式为,X22-的电子式为;
(5)写出与XY电子总数相同的一种双原子核微粒的化学式。