早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔融)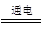 4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH
4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH 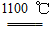 Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
| A.电解熔融氢氧化钠制钠,阳极发生的电极反应为2OH--2e-=H2↑+O2↑ |
| B.若用戴维法与吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| C.吕萨克法制钠的原理是利用铁的还原性比钠强 |
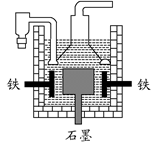
| D.目前工业上常用电解熔融氯化钠法制钠(如下图),电解槽中石墨为阳极,铁为阴极 |
下表为某有机物与各种试剂的反应现象,则这种有机物可能是
| 试剂 |
钠 |
溴水 |
NaHCO3溶液 |
| 现象 |
放出气体 |
褪色 |
放出气体 |
A.CH2===CH—CH2—OH
B.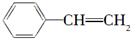
C.CH2===CH—COOH
D.CH3COOH

 下列各组物质互为同系物的是
下列各组物质互为同系物的是
| A.CH4与C2H4 |
B.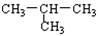 与 CH3-CH2-CH2-CH3 与 CH3-CH2-CH2-CH3 |
| C.C2H6与C3H8 |
| D.O2与O3 |
为提纯下列物质(括号内的物质为杂质),所用的除杂试剂和分离方法都正确的是
| 选项 |
A |
B |
C |
D |
| 被提纯物质 |
酒精(水) |
乙醇(乙酸) |
乙烷(乙烯) |
溴苯(溴) |
| 除杂试剂 |
生石灰 |
氢氧化钠溶液 |
酸性高锰酸钾溶液 |
KI溶液 |
| 分离方法 |
蒸馏 |
分液 |
洗气 |
分液 |
右图是某有机分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。该物质不具有的性质是
| A.与氢氧化钠反应 | B.与稀硫酸反应 |
| C.发生酯化反应 | D.使紫色石蕊变红 |
下列方程式书写正确的是
A.碳酸的电离方程式:H2CO3 2H+ + CO32- 2H+ + CO32- |
B.硫化钠水解: S2-+2H2O H2S +2OH- H2S +2OH- |
| C.往AgI悬浊液中滴加Na2S饱和溶液:2Ag+ (aq)+ S2-(aq) = Ag2S(s) |
| D.用醋酸除水垢: 2CH3COOH + CaCO3= 2CH3COO-+ Ca2++ H2O + CO2↑ |