对反应:A+B AB来说,常温下按以下情况进行反应:
AB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol
②50 mL溶液中含A、B各0.05 mol
③0.1 mol·L-1的A、B溶液各10 mL
④0.5 mol·L-1的A、B溶液各50 mL
四种溶液反应速率的大小关系是( )
A.②>①>④>③ B.④>③>②>①
C.①>②>④>③ D.①>②>③>④
下列离子方程式表达正确的是( )
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+ Fe3++3H2O Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HC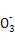 +H2O +H2O H3O++C H3O++C |
C.稀硝酸中加入足量的铁屑:3Fe+8H++2N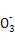  3Fe2++2NO↑+4H2O 3Fe2++2NO↑+4H2O |
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:N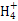 +Al3++2S +Al3++2S +2Ba2++5OH- +2Ba2++5OH- Al Al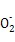 +2BaSO4↓+NH3·H2O+2H2O +2BaSO4↓+NH3·H2O+2H2O |
下表中有关离子方程式的评价合理的是( )
| 选项 |
化学反应及离子方程式 |
评价 |
| A |
AlCl3溶液中加入过量氨水: Al3++3NH3·H2O  Al(OH)3↓+3N 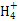 |
错误,铝元素的产物应该是Al 或[Al(OH)4]- |
| B |
过量氯气通入溴化亚铁溶液中: 3Cl2+2Fe2++4Br-  6Cl-+2Fe3++2Br2 6Cl-+2Fe3++2Br2 |
正确 |
| C |
用氨水吸收过量二氧化硫: 2NH3·H2O+SO2  2N 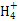 +S +S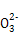 十H2O 十H2O |
正确 |
| D |
氯化铵溶于水: N 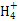 +2H2O +2H2O H3O++NH3·H2O H3O++NH3·H2O |
错误,氯化铵溶解于水是物理变化,不能写离子方程式 |
下列各组离子在指定条件下能大量共存的是( )
①漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+
②滴加石蕊试液呈红色的溶液:K+、N 、Cl-、S2-
、Cl-、S2-
③常温下能够与金属Mg反应放出气体的溶液:Fe3+、Al3+、S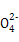 、K+
、K+
④常温下pH=2的溶液中:N 、Na+、Cl-、Cu2+
、Na+、Cl-、Cu2+
⑤无色溶液中:K+、CH3COO-、HC 、Mn
、Mn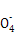
| A.②③ | B.①③ | C.③④ | D.①⑤ |
化学用语是学习化学的工具和基础。下列有关化学用语的使用正确的是( )
A.用食醋除去水壶内的水垢:CaCO3+2H+ Ca2++CO2↑+H2O Ca2++CO2↑+H2O |
B.纯碱溶液呈碱性的原因是:C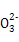 +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
C.钢铁发生吸氧腐蚀的正极反应式: +4e-+2H2O +4e-+2H2O 4OH- 4OH- |
D.表示氢气燃烧热的热化学方程式为2H2(g)+O2(g) 2H2O(l) ΔH="-571.6" kJ· mol-1 2H2O(l) ΔH="-571.6" kJ· mol-1 |
下表对某些反应方程式的评价合理的是( )
| 编号 |
实验 |
离子方程式或电极反应式 |
评价 |
| A |
次氯酸钙溶液中通入足量SO2 |
Ca2++ClO-+SO2+H2O CaSO4↓+Cl-+2H+ CaSO4↓+Cl-+2H+ |
正确 |
| B |
Ba(OH)2溶液中加入过量Al2(SO4)3溶液 |
3Ba2++6OH-+2Al3++3S  3BaSO4↓+2Al(OH)3↓ 3BaSO4↓+2Al(OH)3↓ |
正确 |
| C |
醋酸铵溶于水 |
CH3COO-+N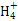  CH3COOH+NH3·H2O CH3COOH+NH3·H2O |
错误,阴阳离子水解相互促进,应该用“ ”号 ”号 |
| D |
用惰性电极电解氯化铜和氯化钠的混合溶液一段时间 |
阴极:Cu2++2e- Cu Cu阳极:4OH--4e-  2H2O+O2↑ 2H2O+O2↑ |
错误,只因为两极得失电子没配平 |