对于反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3 kJ·mol-1,且熵减小,在常温常压下该反应能自发进行,对反应的方向起决定作用的是( )
| A.焓变 | B.温度 | C.压强 | D.熵变 |
1mol丙烯与Cl2发生加成反应,得到的产物再与Cl2发生取代反应,两个过程最多消耗Cl2的物质的量为()
| A. 2mol | B.4 mol | C.7mol | D.8 mol |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是()
| A.0.1molC3H6Cl2中化学键总数为NA |
| B.42g乙烯中含碳原子数为3NA |
| C.标准状况下,1L苯完全燃烧生成的气态产物的分子数为(6/22.4)NA |
| D.0.1mol乙醇完全燃烧所消耗的氧分子数一定为0.3NA |
下列各组物质中,互称同系物的是()
A.CH3-CH=CH2和 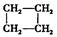 |
B.苯和间二甲苯 |
| C.氯仿和氯乙烷 | D.2—丙醇和丙二醇 |
下列有机物命名不正确的是()
| A. |
 |
丁烯 |
| B. |
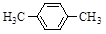 |
对二甲苯 |
| C. |
  CH3CH3 CH3CH3 CH3-CH-CH2-CH2-C-CH2-CH3 CH3-CH-CH2-CH2-C-CH2-CH3OH |
2,5—二甲基—5—庚醇 |
| D. |
CH3CH(C2H5)CH(CH3)2 |
2,3—二甲基戊烷 |
下列有关化学用语使用正确的是()
A.CH4分子的比例模型: |
B.乙醇的分子式CH3CH2OH |
| C.苯的最简式 C6H6 | D.乙烯的结构简式CH2CH2 |