下列书写的离子方程式中,正确的是
| A.高锰酸钾溶液与乙二酸(草酸)反应:2MnO4-+5C2O42-+16H+®2Mn2++10CO2↑+8H2O |
| B.在NH4HSO4溶液中慢慢滴入等物质的量的NaOH溶液:NH4++OH-®NH3·H2O |
| C.VO2+与酸性高锰酸钾溶液反应:5VO2++MnO4-+H2O®5VO2++Mn2++2H+ |
| D.Fe2+离子被空气氧化:4Fe2++O2+2H2O®4Fe3++4OH- |
对下列物质:①H2SO4、②CO2、③NaOH、④BaSO4、⑤NH3、⑥SO2、⑦NH3·H2O 、⑧C2H5OH、⑨Cu、⑩氯化钠溶液按要求分类不正确的是
| A.弱电解质:④、⑦ | B.电解质:①、③、④、⑦ |
| C.非电解质:②、⑤、⑥、⑧ | D.强电解质:①、③、④ |
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示。下列说法中不正确的是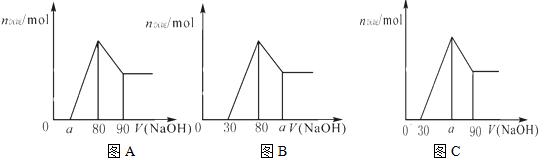
A.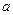 的取值范围为0 的取值范围为0 ≤a<50 ≤a<50 |
B.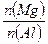 的最大值为2.5 的最大值为2.5 |
C.若将关系图改为B图时,则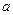 的取值范围为80<a<90 的取值范围为80<a<90 |
D.若将关系图改为C图时,则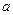 的取值范围为75<a<90 的取值范围为75<a<90 |
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物, 根据下列四种金属的熔沸点:
根据下列四种金属的熔沸点:
| Na |
Cu |
Al |
Fe |
|
| 熔点(0C) |
97.5 |
1083 |
660 |
1535 |
| 沸点(0C) |
883 |
2595 |
2200 |
3000 |
其中不能形成合金的是
A.Cu和Al B.Fe和Cu C.Fe和Na D.Al和Na[
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由H+(aq)+OH-(aq)===H2O(l)△H=-57.3kJ·mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ |
| C.由C(石墨)="=" C(金刚石)△H= +1.90 kJ·mol-1可知,金刚石比石墨稳定 |
D.500℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6kJ·mol-1 2NH3(g)△H=-38.6kJ·mol-1 |
将mg钠和铝的混合物放入ng水中,待反应停止后,得到ag沉淀,则滤液中的溶质是
| A.NaAlO2 | B.NaAlO2和NaOH | C.Al(OH)3 | D.NaOH |