将浓度为0.1mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B.Ka(HF) | C.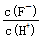 |
D. |
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示。下列关于整个反应过程中的叙述错误的是
| A.Oa段反应的化学方程式是Ba(OH)2+CO2 =BaCO3↓+H2O |
| B.bc段与cd段所消耗CO2的体积相同 |
| C.bc段反应的离子方程式是2AlO2-+3H2O+CO2 = 2Al(OH)3↓+CO32- |
| D.de段沉淀减少是由于BaCO3固体的消失 |
铁、铜混合粉末18.0g加入到100mL 5.0 mol/L FeCl3溶液中,剩余固体质量为3.2g,下列说法正确的是
| A.剩余固体是铁、铜混合物 |
| B.反应后溶液中n(Fe2+)+ n(Cu2+)="0.75" mol |
| C.反应后溶液中n(Fe3+)="0.10" mol |
| D.原固体混合物中铜的质量是8.0g |
两种金属混合物共15g,投入足量的盐酸中,充分反应得11.2L H2(标准状况),则原混合物组成中肯定不能为下列的
| A.Mg、Ag | B.Fe、Mg | C.Al、Zn | D.Mg、Al |
除去下列括号内的杂质,所加试剂和操作均正确的是
| 选项 |
需除杂的物质 |
试剂 |
操作 |
| A |
NaCl(Na2CO3) |
稀盐酸 |
蒸发结晶 |
| B |
CO2(HCl) |
饱和Na2CO3溶液 |
洗气 |
| C |
Cl2(H2O) |
碱石灰 |
洗气 |
| D |
CO2(CO) |
———— |
点燃 |