实验室里常用锌和稀硫酸反应来制取氢气。林辉同学取6.5 g锌并加入50 g一定质量分数的硫酸溶液,恰好完全反应后,得到56.3 g硫酸锌溶液。发生反应的化学方程式是:
Zn+H2SO4=ZnSO4+H2↑。请你计算:
(1)生成氢气的质量为 g。
(2)硫酸溶液中溶质的质量分数。
根据
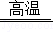 反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁 的生铁的质量是多少?
(1)用 克溶质质量分数为 的过氧化氢溶液配制成溶质质量分数为 的过氧化氢溶液,需加水_____克。
(2)取 克某过氧化氢溶液放入锥形瓶中并加入一定量的二氧化锰,用电子秤测其质量,不同时间电子秤的读数如下表所示。试计算该过氧化氢溶液的溶质质量分数(不考虑 逸出,写出计算过程,结果保留到 )。
|
反应时间/ |
|
|
|
|
|
|
|
|
锥形瓶+瓶内物质的总质量/ |
|
|
|
|
|
|
|
硫酸铜对过氧化氢( )的分解有催化作用。取8.5%的过氧化氢溶液40g倒入锥形瓶中,向其中加入15%的硫酸铜溶液6.6g,使过氧化氢完全分解,若产生的气体全部逸出,请计算:
(1)过氧化氢的相对分子质量为 。
(2)产生氧气的质量(写出计算过程)。
(3)反应后所得硫酸铜溶液中溶质的质量分数为 。
向氯化铜和盐酸的混合溶液中滴加一定溶质质量分数的氢氧化钡溶液,充分搅拌,加入氢氧化钡溶液的质量与生成沉淀的质量关系如图所示。
请完成下列问题:
(1)a点时,溶液的pH 7。
(2)求所用氢氧化钡溶液中溶质的质量分数。(写出计算过程)

游览活动即将结束,化学精灵请同学们乘坐氢燃料汽车回家。氢气作为燃料具有热值高、无污染的优点,但是制备成本高,储存有难度。若用废旧黄铜( 合金)和稀硫酸为原料制备氢气,测得实验数据如图,请计算:
(1)该废旧黄铜中锌的质量为_____ 。
(2)实验中生成氢气的质量。
