已知33As、35Br位于同一周期。下列关系正确的是( )。
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4>H2SO4>H3PO4 |
NA代表阿伏加德罗常数的数值,下列说法正确的是
| A.1mol FeCl3完全水解生成NA个胶体粒子 |
| B.常温常压下,23g NO2分子总数小于0.5NA |
| C.标准状况下,2.24 L的CCl4中含有的C—Cl键数为0.4NA |
| D.6.8g熔融态KHSO4中含有0.1NA个阳离子 |
通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
| 化学键 |
Si—O |
Si—Cl |
H—H |
H—Cl |
Si—Si |
Si—C |
| 键能/kJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热△H为
Si(s)+4HCl(g),该反应的反应热△H为
A.+236 kJ·mol-1B.-236 kJ·mol-1
C.+412 kJ·mol-1 D.-412 kJ·mol-1
下列说法正确的是
| A.图I所示装置用于Cu和浓H2SO4制取少量的SO2气体 |
| B.图Ⅱ用于吸收HCl气体能防倒吸 |
| C.图Ⅲ可用于收集气体H2、CO2、Cl2、NH3 |
| D.图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化 |
下列离子或分子组中,在相应的环境中能大量共存的是
一未完成的离子方程式:________+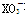 +6H+===3X2+3H2O,据此判断下列说法正确的是
+6H+===3X2+3H2O,据此判断下列说法正确的是
| A.X原子最外层有5个电子 |
| B.当有1molX2生成时,共有2mol电子转移 |
| C.氧化产物和还原产物的物质的量之比为5∶1 |
D.“_____”上所填的微粒和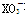 在任何环境下都不能共存 在任何环境下都不能共存 |