工业上可用二氧化硫生产硫酸,反应的化学方程式为2SO2 + O2 + 2H2O = 2H2SO4。欲将16吨二氧化硫气体完全转化为硫酸,则参加反应的氧气的质量是多少?
为测定某纯碱(
)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取
试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至
时,烧杯内溶液的总质量为
(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算: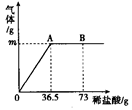
(1)
点产生气体的质量为;
(2)试样中碳酸钠的质量分数(结果精确到0.1%);
(3)
点时,烧杯内溶液中溶质的化学式。
小明同学将
含杂质的的纯碱样品(碳酸钠与氯化钠的混合物)与
稀盐酸相混合,充分反应,测得反应生成气体的质量(
)与反应时间(
)的数据如下表所示:
| 反应时间 | |||||||
| 气体质量 | 0 |
0.88 |
1.76 |
2.64 |
3.52 |
4.4 |
4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成
的质量为
.
(2)请在下面的坐标图中,画出反应时生成气体的质量(
)随时间(
)变化的曲线。
(3)求完全反应后所得溶液中溶质的质量分数。(
↑)。
现有200 溶质质量分数为10%的硝酸钾溶液,若使溶液的溶质质量分数增加一倍,因向溶液加入硝酸钾 ,或蒸发掉水 。
26 黄铜( 合金)与100 稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8克。求:
⑴黄铜中铜的质量分数;
⑵反应后所得溶液中溶质质量分数。(计算结果精确到0.1%)
实验室常用右下图所示装置测定空气中氧气含量。
(1)若有1.24
红磷发生反应,则根据化学方程式计算,产生的固体(
)有多少克?
(2)该试验中红磷过量,你认为是否有道理?(填"是"或"否"),你的理由是。
(3)在动手实验的过程中,你认为该实验的不足是(至少一条)