把一块镁铝合金投入到20 mL 1 mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的关系如图所示。下列说法中正确的是( )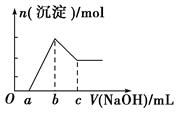
| A.镁铝合金具有很强的抗腐蚀能力,它不溶解在任何酸、碱或盐中 |
| B.c值越大,合金中Al的含量越高 |
| C.b值越大,合金中Mg的含量越高 |
| D.假设c=25,整个反应过程中,主要发生了5个离子反应 |
下列措施不符合节能减排的是
| A.大力发展火力发电,解决电力紧张问题 |
| B.在屋顶安装太阳能热水器为居民提供生活用热水 |
| C.用石灰对煤燃烧后形成的烟气脱硫,并回收石膏 |
| D.用杂草、生活垃圾等有机废弃物在沼气中发酵产生沼气,作家庭燃气 |
还原2.4×10-3 mol [XO(OH)3]+ 到X元素的低价态时,消耗0.2mol·L—1的Na2SO3溶液30 mL,则X元素反应后的价态是
| A.-1 | B.+1 | C.0 | D.-2 |
将铝粉与某铁的氧化物FeO·2Fe2O3粉末配制成铝热剂,分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
| A.11.20L | B.15.68L | C.22.40L | D.31.36L |
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4==2NaHSO4+MnsO4+2H2O+I2
②2NaIO3+5NaHSO3==2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中NaHSO4均为氧化产物 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
C.氧化性:MnO2>SO >IO >IO >I2 >I2 |
| D.反应①、②中生成等量的I2时转移电子数比为1:5 |
等质量的下列物质与足量浓盐酸反应,放出Cl2物质的量最多的是
| A.KMnO4 | B.MnO2 | C.NaClO3 | D.NaClO |