密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g) CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是( )
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是( )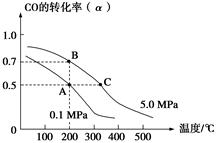
A.若A、B两点表示在某时刻达到的平衡状态,此时A、B两点时容器中,n(A)总∶n(B)总=4∶5
B.若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA<tC
C.设B、C两点的平衡常数分别为KB、KC,则KB<KC
D.在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率
把wg铁粉和铝粉的混合物溶于足量盐酸中,再加入过量的 NaOH溶液,然后过滤,将沉淀完全收集后,放蒸发皿中加热,直至被加热的物质质量不再变化,取出蒸发皿中的物质称量仍为wg。求原混合物中铝粉的质量分数是
| A.30% | B.50% | C.70% | D.90% |
若100mL0.1mol/L硫酸铝溶液和氢氧化钠溶液反应,得到1.17g沉淀,则需0.5mol/L的NaOH溶液的体积为
| A.230mL | B.100mL | C.90mL | D.50.3mL |
下列离子在溶液中能大量共存的是
A. |
B. |
C. |
D. |
下列离子方程式书写正确的是
| A.铝粉投入到NaOH溶液中:2Al+2OH-══2AlO2-+H2↑ |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH-══ Al(OH)3↓ |
C.三氯化铁溶液中加入铁粉: |
| D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
过量的NaHCO3和Na2O2混合,在密闭容器中充分混合加热后,最后排出气体,残留的固体是
| A.Na2O | B.Na2CO3 | C.Na2O2和Na2CO3 | D.Na2O2和Na2O |