常温下,向100 mL 0.1 mol·L-1 H2A(二元酸)溶液中逐滴加入0.2 mol·L-1 NaOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列有关说法正确的是( )
| A.H2A为二元强酸 |
| B.N点对应溶液有:c(Na+)=c(A2-)+c(HA-) |
| C.K点对应溶液中离子浓度由大到小的顺序为c(A2-)>c(Na+)>c(OH-)>c(H+) |
| D.K点时加水稀释溶液,c(H+)增大 |
对于蔗糖的说法中,不正确的是( )
| A.蔗糖是最重要的二糖,它的式量是葡萄糖式量的2倍 |
| B.纯净的蔗糖溶液中加入银氨溶液,微热,不发生银镜反应 |
| C.在蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,再水浴加热,看不到有银镜生成 |
| D.在蔗糖里加入浓硫酸,可观察到颜色变黑,并有泡沫出现 |
下列关于葡萄糖与果糖的说法不正确的是( )
| A.两者互为同分异构体 |
| B.两者都易溶于水 |
| C.两者都能发生银镜反应 |
| D.葡萄糖比果糖甜 |
A、B两瓶液体,一瓶是植物油,一瓶是矿物油。现各取少量,放在两支洁净的试管里,加入NaOH溶液并加热,冷却后加水振荡静置,A出现泡沫,B无泡沫且分为两层。
由此可推出,A为________,B为________。
理由是___________________________________________。
天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11)。该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如下图所示(注意图中的反应式不完整)。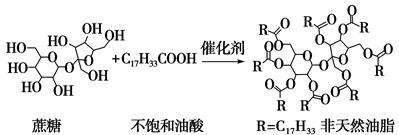
下列说法正确的是( )
| A.蔗糖酯也是高级脂肪酸的甘油酯,属于油脂类物质 |
| B.该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应 |
| C.非天然油脂为高分子化合物 |
| D.该蔗糖酯在稀硫酸的作用下水解,最终可生成三种有机化合物 |
某物质的结构为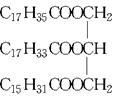 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )
| A.一定条件下与氢气反应可以生成硬脂酸甘油酯 |
| B.一定条件下与氢气反应可以生成软脂酸甘油酯 |
| C.与氢氧化钠溶液混合加热能得到肥皂的主要成分 |
| D.与其互为同分异构体且完全水解后产物相同的油脂有三种 |