已知:①CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH1=-Q1
CO2(g)+2H2O(l) ΔH1=-Q1
②H2(g)+O2(g) H2O(g) ΔH2=-Q2
H2O(g) ΔH2=-Q2
③H2(g)+O2(g) H2O(l) ΔH3=-Q3,常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况),经完全燃烧恢复到常温,放出的热量是( )
H2O(l) ΔH3=-Q3,常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况),经完全燃烧恢复到常温,放出的热量是( )
| A.0.4Q1+0.05Q2 | B.0.4Q1+0.1Q2 |
| C.0.4Q1+0.05Q3 | D.0.4Q1+0.1Q3 |
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-57.3 kJ·mol-1,则HCN在水溶液中电离的ΔH等于( )。
| A.-69.4 kJ·mol-1 | B.-45.2 kJ·mol-1 |
| C.+45.2 kJ·mol-1 | D.+69.4 kJ·mol-1 |
在一定条件下A与B反应可生成C和D,其能量变化如图: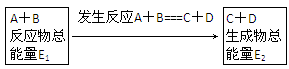
下列有关反应A+B=C+D的说法正确的是( )。
| A.反应前后原子的种类和数目一定不变 |
| B.反应前后分子的种类和数目一定改变 |
| C.反应物的总能量E1与生成物的总能量E2一定相等 |
| D.此反应一定有热量的变化 |
下列与化学反应能量变化相关的叙述正确的是( )。
| A.生成物总能量一定低于反应物总能量 |
| B.酒精可用作燃料,说明酒精燃烧是释放能量的反应 |
| C.干冰气化需要吸收大量的热,这个变化是吸热反应 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是( )。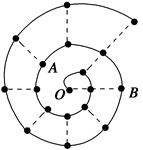
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.B元素是图中金属性最强的元素
D.A、B组成的化合物中可能含有共价键
下列有关原子结构及元素周期律的叙述正确的是( )。
| A.同主族元素的原子最外层电子数相同,化学性质也相同 |
| B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |