下列图示与对应的叙述相符的是( )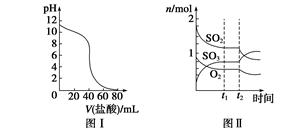
| A.图Ⅰ表示常温下盐酸滴加到0.1 mol·L-1某碱溶液中得到的滴定曲线,由图Ⅰ可知二者恰好中和时,所得溶液的pH>7 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度 |
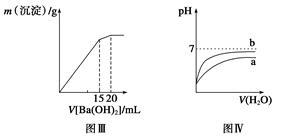
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时,沉淀全部是BaSO4 |
| D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
将锌片和铜片用导线连接后放入稀硫酸溶液中,发生原电池反应,
下列叙述错误的是
| A.溶液的pH增大 | B.溶液中的Zn2+浓度增大 |
| C.溶液中的SO42-浓度增大 | D.溶液的密度增大 |
已知:①能量越低的物质越稳定,②白磷转化成红磷放出热量。
据此,下列判 断或说法中正确的是
| A.在相同的条件下,红磷比白磷稳定 |
| B.在相同的条件下,白磷比红磷稳定 |
| C.红磷和白磷的结构相同 |
| D.红磷容易发生自燃而白磷则不会自燃 |
某种元素R的核外电子数等于核内中子数,取该元素5.6g跟氧气充分反应,可得到12g化合物RO2,则该种元素R在周期表中的位置是
| A.第二周期第ⅣA族 | B.第三周期第ⅣA族 |
| C.第三周期第ⅥA族 | D.第二周期第ⅥA族 |
国际化学组织已将周期表中原主、副族的族号去掉而改称列,如碱金属为第
1列,稀有气体为第18列。按此规定,下列叙述正确的是
| A.第1列元素均能形成M2O和M2O2型化合物 |
| B.第14列元素所形成的化合物种类最多 |
| C.第17列元素均有最高价氧化物R2O7 |
| D.最外层有两个电子的原子都在第2列 |
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3C 2AlN + 3CO↑
2AlN + 3CO↑
下列叙述不正确的是
| A.在氮化铝的合成反应中,N2是还原剂 |
| B.在氮化铝的合成反应中,C是还原剂 |
| C.氮化铝中氮元素的化合价为-3 |
| D.上述反应中每生成1molAlN,转移3 mol e- |