已知C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH1=-a kJ/mol
C2H5OH(g)=C2H5OH(l) ΔH2=-b kJ/mol
H2O(g)=H2O(l) ΔH3=-c kJ/mol
若使92 g酒精液体完全燃烧,最后恢复到室温,则放出的热量(单位kJ)为( )
| A.4a+4b+4c | B.2a-2b+6c |
| C.2a-2b+2c | D.2a-6b+2c |
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示,下列说法中不正确的是
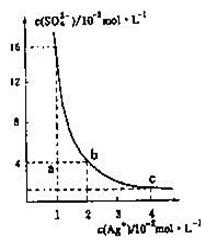
| A.b点对应的Ksp等于c点对应的Ksp |
| B.采取蒸发溶剂的方法可以使溶液从a点变到b点 |
| C.该温度下,Ag2SO4的溶度积常数(Ksp)为1.6×10-5(mol·L-1)3 |
| D.0.02mol·L-1的AgNO3溶液与的0. 2mol·L-1的Na2SO4溶液等体积混合不会生成沉淀 |
元素周期律为人们寻找新材料提供了科学的途径。下列说法不正确的是
A、在IA族可以找到光电材料
B、在IIIA、IVA、VA族可以找到优良的半导体材料
C、在IB、IIB、IIIB族可以找到高温超导材料
D、在VIII族可以找到新型农药材料
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是
| A.Z2Y | B.X2Y2 | C.Z2Y2 | D.ZYX |
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析正确的是
| A.CuS的溶解度大于PbS的溶解度 |
| B.原生铜的硫化物具有还原性,而铜蓝没有还原性 |
| C.CuSO4与ZnS反应的离子方程式是Cu2++S2-====CuS↓ |
| D.整个过程涉及的反应类型有氧化还原反应和复分解反应 |
下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是
①H2O ②NH3 ③Cl— ④CN— ⑤CO
| A.①② | B.①②③ | C.①②④ | D.①②③④⑤ |