等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得不同时间(t)内产生气体体积(V)的数据如图,根据图示分析实验条件,下列说法中一定不正确的是( )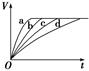
| 组合 |
对应曲线 |
c(HCl)/mol·L-1 |
反应温度/℃ |
铁的状态 |
| 1 |
a |
|
30 |
粉末状 |
| 2 |
b |
|
30 |
粉末状 |
| 3 |
c |
2.5 |
|
块状 |
| 4 |
d |
2.5 |
30 |
块状 |
A.第1组实验中盐酸的浓度大于2.5 mol·L-1
B.第2组实验中盐酸的浓度等于2.5 mol·L-1
C.第3组实验的反应温度低于30 ℃
D.第4组实验的反应速率最慢
下列叙述正确的是( )
| A.同温同压下,4Al(s)+3O2(g)===2Al2O3(s)在常温和点燃条件下的ΔH不同 |
| B.在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应放热,ΔH>0 |
C.已知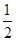 C(s)+ C(s)+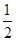 O2(g)=== O2(g)===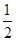 CO2(g) CO2(g)ΔH=-196.8 kJ·mol-1,则碳的燃烧热是ΔH=-196.8 kJ·mol-1 |
| D.已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) |
ΔH=-57.4 kJ·mol-1,则含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的能量
同温同压下,下列热化学方程式中Q值最大的是(均为放热反应)( )
| A.2A(l)+B(l)==="2C(g)" ΔH=-Q1 kJ/mol |
| B.2A(g)+B(g)==="2C(g)" ΔH=-Q2 kJ/mol |
| C.2A(g)+B(g)==="2C(l)" ΔH=-Q3 kJ/mol |
| D.2A(l)+B(l)==="2C(l)" ΔH=-Q4 kJ/mol |
下列反应中反应物总能量高于生成物总能量的是( )
| A.二氧化碳与碳生成一氧化碳 |
| B.碳与水蒸气生成一氧化碳和氢气 |
| C.碳酸钙受热分解 |
| D.盐酸与氢氧化钠反应 |
“能源分类相关图”如图所示,下列四组能源选项中全部符合图中阴影部分的能源是( )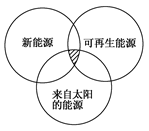
| A.煤炭、石油、潮汐能 |
| B.水能、生物能、天然气 |
| C.太阳能、风能、沼气能 |
| D.地热能、海洋能、核能 |
已知VmL的Fe2(SO4)3溶液中含SO42- a g,取0.25VmL该溶液稀释至4VmL,则稀释后的溶液中Fe3+的物质的量浓度为
A.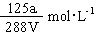 |
B.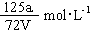 |
C. |
D.以上答案均不正确 |