已知一定温度时发生反应Na2SO4(s)+4H2(g)  Na2S(s)+4H2O(g) ΔH=-225 kJ·mol-1,该反应的正反应速率随时间的变化情况如图所示,在t1时改变了某种条件,反应在t2时达平衡,改变的条件可能是( )
Na2S(s)+4H2O(g) ΔH=-225 kJ·mol-1,该反应的正反应速率随时间的变化情况如图所示,在t1时改变了某种条件,反应在t2时达平衡,改变的条件可能是( )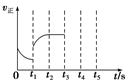
| A.升高温度 | B.增大H2的浓度 |
| C.使用催化剂 | D.增大压强 |
| A.c(Na+)>c(HCOO-)>c(OH-)>c(H+) |
| B.c(HCOO-)>c(Na+)>c(OH-)>c(H+) |
| C.c(HCOO-)=c(Na+)>c(H+)=c(OH-) |
| D.c(Na+)=c(HCOO-)>c(OH-)>c(H+) |
| A.1.0×10-7 mol·L-1 | B.1.0×10-6 mol·L-1 |
| C.1.0×10-2 mol·L-1 | D.1.0×10-12 mol·L-1 |
| A.c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) |
| B.c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
| C.c(CH3COO-)=c(Cl-)>c(H+)>c(CH3COOH) |
| D.c(Na+)+c(H+)=c(CH3COO-)+c(Cl-)+c(OH-) |
A.c(Na+)=2c(CO ) ) |
B.c(OH-)=2c(H+) |
C.c(HCO )>c(H2CO3) )>c(H2CO3) |
D.c(Na+)<c(CO )+c(HCO )+c(HCO ) ) |
| A |
B |
C |
D |
|
| H2 |
6 |
1 |
3.5 |
5 |
| N2 |
2 |
0 |
1 |
1.5 |
| NH3 |
0 |
4 |
2 |
1 |
