常温时,下列三种溶液:
①0.001 mol·L-1氨水与0.001 mol·L-1 HCl溶液等体积混合液
②pH=3的HCl与pH=11的NaOH溶液等体积混合液
③pH=11的氨水与pH=3的HCl溶液等体积混合液。
其pH大小关系正确的是( )
| A.①=②=③ | B.①>②=③ |
| C.①<②=③ | D.①<②<③ |
化合物丙由如下反应得到;丙不可能是
| A.CH3CH2CHBrCH2Br | B.CH3CH(CH2Br)2 |
| C.CH3CHBrCHBrCH3 | D.(CH3)2CBrCH2Br |
由苯和液溴反应的原理可推测,若将甲苯与液溴混合,加入铁粉,其反应所得的产物可能有
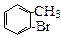 |
|||||||||||||
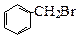 |
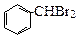 |
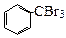 |
|||||||||||
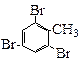 |
|||||||||||||
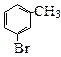 |
|||||||||||||
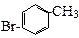 |
|||||||||||||
① ② ③ ④
⑤ ⑥ ⑦
| A.仅①②③ | B.仅⑦ | C.仅④⑤⑥⑦ | D.全部 |
有4种有机物: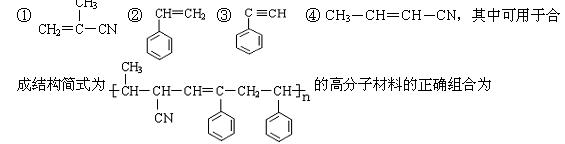
| A.①③④ | B.①②③ | C.①②④ | D.②③④ |
下列各组混合物能用分液漏斗分离的是
| A.硝基苯和苯 | B.苯和甲苯 | C.甘油和水 | D.溴苯和NaOH溶液 |
从石油分馏得到的固体石蜡,用氯气漂白后,燃烧时会产生含氯元素的气体,这是由于石蜡在漂白时与氯气发生了
| A.加成反应 | B.取代反应 | C.聚合反应 | D.催化裂化反应 |