室温时,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的
CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A.若pH>7,则一定是c1V1=c2V2 |
| B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.当pH=7时,若V1=V2,则一定是c2>c1 |
| D.若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+) |
将电解质分为强、弱电解质的依据是
| A.属于离子化合物还是共价化合物 | B.在一定条件下的电离程度 |
| C.熔融状态下是否完全电离 | D.溶于水后的导电能力是强还是弱 |
甲酸是一种有机酸,又叫蚁酸。蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体射入蚁酸,使皮肤红肿、瘙痒,甚至疼痛。要消除这种症状,可在叮咬处涂抹下列物质中的
已知家庭中一些常见物质的pH:食醋-4;牙膏-9;食盐水-7;肥皂水-10;火碱液-13
| A.火碱液 | B.食盐水 | C.牙膏或肥皂水 | D.食醋 |
(8分)2013年以来全国各地都遭遇“十面霾伏”。其中,二氧化硫、氮氧化物和可吸入颗粒物是雾霾的主要组成成分。综合治理其污染是环境化学当前的重要研究内容。
(1)NO2有较强的氧化性,能将SO2氧化生成SO3,本身被还原为NO,已知下列两反应过程中能量变化如图所示: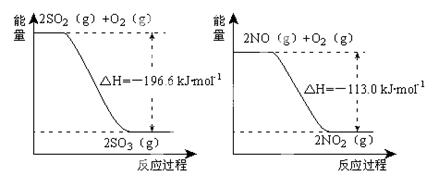
则NO2氧化SO2的热化学方程式为 _____________________________ 。
(2)SO2与O2反应时的平衡转化率与温度、压强的关系如图所示。根据图示回答下列问题:
①压强:Pl P2(填“>”、“=”或“<”)。
②平衡常数:A点B点(填“>”、“=”或“<”)。
③200℃下,将一定量的SO2和O2充人体积为1 L的密闭容器中,经10min后测得容器中各物质的物质的量如下表所示:
| 气体 |
SO2 |
O2 |
SO3 |
| 物质的量(mol) |
1.6 |
1.8 |
0.4 |
10min内该反应的反应速率v(O2)=;该反应达到化学平衡状态的标志是。
a.SO2和O2的体积比保持不变 b.体系的压强保持不变
c.混合气体的密度保持不变 d.SO2和SO3物质的量之和保持不变
(3)用NH3催化还原NOx可以消除氮氧化物的污染。
①写出氨气消除NO污染的化学方程式 ___________________________;
②若还原产物比氧化产物多0.5mol,则反应转移电子数为 ________。
某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下、
该同学得出的结论正确的是
| A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素 |
| B.根据现象2可推出该固体粉末中一定含有NaNO2 |
| C.根据现象3可推出该固体粉末中一定含有Na2SO4 |
| D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3 |
向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)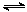 xC(g),△H<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g),△H<0。测得两容器中c(A)随时间t的变化如图所示: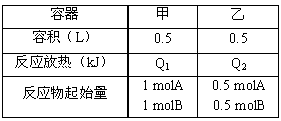

下列说法正确的是
A.x="1"
B.Q1=2Q2
C.根据题中信息无法计算a值
D.保持其他条件不变,起始时向乙容器充入0.2 mol A、0.2 mol B、0.2 mol C,则此时v(正)> v(逆)