室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是( )
| A.a点由水电离出的c(H+)=1×10-14 mol/L |
| B.b点:c(NH4+)+c(NH3·H2O)=c(Cl-) |
| C.c点:c(Cl-)=c(NH4+) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
下列结论错误的是( )
①微粒半径:r(K+)>r(Al3+)>r(S2-)>r(Cl-) ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③还原性:S2->Cl->Br->I-④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
| A.① | B.①③ | C.②③④⑤⑥⑦ | D.①③⑤ |
在一定温度下,下列叙述不是可逆反应A(g)+3B(g) 2C(g)达平衡时的特征的是( )
2C(g)达平衡时的特征的是( )
(1)C的生成速率与C的分解速率相等; (2)单位时间内生成amol A,同时生成3amolB;
(3)A、B、C的浓度不再变化;(4)A、B、C的压强不再变化;
(5)混合气体的总压不再变化;(6)混合气体的物质的量不再变化;
(7)单位时间内消耗amolA,同时生成3amolB;(8)A、B、C的分子数之比为1:3:2。
A.(3)(8) B.(1)(6) C.(2)(4) D.(2)(8)
可逆反应mA(g)+nB(g) pC(g)+gD(g)的v-t图象如下图甲,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如下图乙。()
pC(g)+gD(g)的v-t图象如下图甲,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图象如下图乙。()
①a1=a2②a1<a2③b1=b2④b1<b2⑤t1>t2⑥t1=t2
⑦两图中阴影部分面积相等⑧乙图阴影部分面积更大,以上正确的为( )
| A.①③⑥⑦ | B.①④⑥⑧ | C.②③⑤⑧ | D.②④⑤⑦ |
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法不正确的是 ()
①在标准状况下,每消耗5.6L CH4可以向外电路提供2mole-
②通过甲烷电极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
③通过甲烷的电极为电池的正极,通过氧气的电极为负极
④电池放电后,溶液PH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是 ( )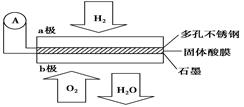
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-―→4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |