已知在常温下测得浓度均为0.1 mol·L-1的下列三种溶液的pH:
| 溶质 |
NaHCO3 |
Na2CO3 |
NaCN |
| pH |
9.7 |
11.6 |
11.1 |
下列说法中正确的是( )
A.阳离子的物质的量浓度之和:
Na2CO3>NaCN>NaHCO3
B.相同条件下的酸性:H2CO3<HCN
C.三种溶液中均存在电离平衡和水解平衡
D.升高Na2CO3溶液的温度, 减小
减小
设NA为阿伏加德罗常数。下列说法中正确的是
| A.1molNH4+中含有10NA个质子 |
| B.t℃时,1LpH=6的纯水中,含1×10-6 NA个OH- |
| C.78gNa2O2中含阴离子的数目为2 NA |
| D.向FeI2溶液中通入适量氯气,当有1molFe2+被氧化时,总共转移电子的数目为1 NA |
某有机物结构简式为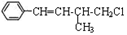 ,下列叙述不正确的是
,下列叙述不正确的是
| A.1mol该有机物在加热和催化剂作用下,最多能和4 molH2反应 |
| B.该有机物能使溴水褪色也能使酸性KMnO4溶液褪色 |
| C.该有机物遇硝酸银溶液产生白色沉淀 |
| D.该有机物在一定条件下,能发生消去反应或取代反应 |
已知1mol白磷变成1mol红磷时放出热量18.39kJ,则下列两个反应中:
4P(白,s)+5O2(g)=2P2O5(s)△H=-Q1kJ/mol
4P(红,s)+5O2(g)=2P2O5(s)△H=-Q2kJ/mol
Q1和Q2的关系正确的是
| A.Q1= Q2 | B.Q1>Q2 | C.Q1<Q2 | D.无法确定 |
下列离子方程式表达正确的是
| A.鸡蛋壳浸泡在盐酸中产生气泡:CO32-+2H+=CO2↑+H2O |
| B.四氧化三铁固体溶解在稀硝酸溶液中:Fe3O4+8H+=2Fe3++Fe2++4H2O |
| C.将氨气通入硫酸溶液中:NH3 + H+ = NH4+ |
| D.向碳酸氢铵溶液中加入足量的NaOH溶液:NH4+ +OH-= NH3·H2O |
关于Na2CO3和NaHCO3比较中,下列说法不正确的是
| A.NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解 |
| B.等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多 |
| C.等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深 |
| D.Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同 |