近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化
学方程式为:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2 X ”。这个化学方程式中
最后一种物质X的化学式是: 。
(2)“二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊。”请写出二氧化硫与澄清石灰水反应的化学方程式: 。并写出实验室制取二氧化碳的化学方程式: 。
根据上述资料,甲同学、乙同学和丙同学分别设计实验方案进行探究。
【实验探究】(3)甲同学:“实验操作”:甲同学进行了如下图所示A、B两步实验: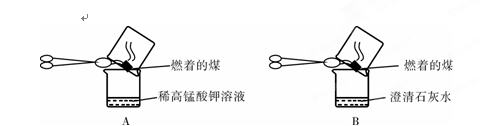
“实验现象”: A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(4)乙同学认为甲同学的实验方案不合理,其理由是: 。
(5)丙同学:
“实验操作”:丙同学进行了如下图所示实验(部分装置在图中略去):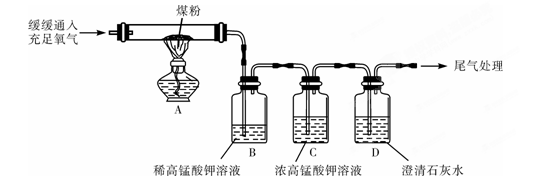
【探究与结论】(6)上图C装置的作用是 。
(7)要证明煤中含有碳元素和硫元素的现象是:丙同学的实验中 。
【2015年福建省厦门市】有关NaOH与CO2反应的探究
探究一:检验NaOH固体样品露置空气中一段时间后的成分
【查阅资料】Na2CO3溶液是碱性;KCl溶液、BaCl2溶液显中性、BaCO3难溶于水。
(1)检验样品是否变质。检验样品成分中是否含碳酸根的实验方法(操作、现象及结论):
___________________________________________________________________________。
(2)检验样品是否完全变质。实验操作:取样品加水溶解,先加过量的_________(填编号,下同),再滴加________。
| A.盐酸 | B.KCl溶液 | C.BaCl2溶液 | D.Ba(OH)2溶液 E.酚酞试液 |
探究二:用NaOH溶液测定空气中酸性气体(CO2、SO2)的体积分数
【实验装置】如图所示,向细玻璃管内注入少量水,形成一段水柱;经检查该装置气密性良好。已知细玻璃管单位长度的容积为0.1mL·cm—1。水柱的质量忽略不计。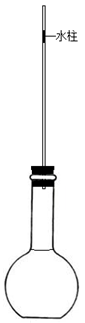
【操作步骤】保持外界条件不变,完成以下操作:
①将40mL浓NaOH溶液迅速倒入烧瓶内,立即塞紧橡皮塞,并在细玻璃管上标记水柱底部的位置
②观察并测量得出水柱缓慢向下移动的距离为2.0cm;
③实验结束后,根据①中的标记,测得该标记以下细玻璃管及烧瓶的总容积为340mL。
(3)检查图8装置气密性的操作方法:________________________________________。
(4)仅根据本次测量数据,该气体样品中酸性气体的体积分数为________(精确到0.00001)。
(5)在上述操作步骤②中,若装置温度略有升高,实验结果______(填“偏大”、“不变”或“偏小”)。
【2015年广东省】现有工厂丢弃的废铜屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课外活动小组同学欲利用其制取胆矾,他们设计了下面的两种制取流程。
已知Cu+Fe2(SO4)3=2FeSO4+CuSO4 ,请回答: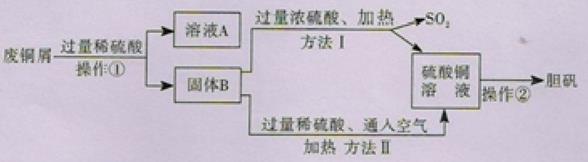
(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ,操作所用到的玻璃仪器有:烧杯、玻璃棒和 。
(2)溶液A的溶质有 (只写一种);铁锈与稀硫酸反应的化学方程式为: 。
(3)两种方法比较,符合绿色化学要求的是方法 ;方法II 的化学方程式为:
2Cu + 2H2SO4 + = 2CuSO4 + ,操作‚实验步骤为: ,
降温结晶。
【2015年湖北省襄阳市】某兴趣小组发现了一包敞口放置的碱石灰样品,为探究其成分,同学们在实验室对这包碱石灰样品展开了探究。
【查阅资料】①碱石灰是由CaO和NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体。②熟石灰微溶于水,且溶于水放出的热量很少可以忽略不计。③BaCl2溶液显中性。
【提出猜想】根据资料,同学们分析碱石灰样品的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和 。
【实验探究】小组讨论后设计如下实验进行探究:
| 实验步骤及操作 |
实验现象 |
结论 |
| ①取部分该样品于试管中,加少量水 |
无明显放热现象 |
碱石灰样品中不含CaO 和 |
| ②继续加足量水,振荡,静置 |
产生白色沉淀 |
样品中一定含有CaCO3 |
| ③从步骤②的试管中取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液 |
产生白色沉淀 |
|
| ④将步骤③所得物质过滤,向滤液中滴加无色酚酞溶液 |
溶液变红色 |
【思考与分析】
小杰同学经过分析认为步骤②的结论不准确,原因是 (用化学方程式表示)。
【解释与结论】
通过以上探究与分析:可以得出该碱石灰样品一定含有的物质是 ;实验探究步骤④所得溶液中除酚酞外还含有的溶质有 。
【2015年湖北省孝感市】做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究。
【提出问题】溶液中的溶质是什么物质?
【作出猜想】(1)甲同学认为溶液中的溶质只有Na2SO4一种物质。
(2)乙同学认为溶液中的溶质是Na2SO4和 两种物质。
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质。
【查阅资料】①Na2SO4溶液显中性。
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质。
【实验验证】
| 实验操作 |
实验现象 |
实验结论 |
|
| 乙同学 实验 |
取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 |
铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 |
猜想(2)成立 |
| 丙同学 实验 |
取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 |
溶液变 色 |
猜想(3)成立 |
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立。经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是 。兴趣小组的同学经过充分讨论,一致认为猜想(3)成立。
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液? (填“能”或“不能”)
(2)乙同学的实验中铝片与 溶液发生了反应,请写出铝与该溶液发生反应的化学方程式 。
【2015年湖南省益阳市】某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖。对于该溶液是否变质,同学们开始实验探究。
【猜想假设】
猜想(1):该溶液没有变质,为NaOH溶液。
猜想(2):该溶液全部变质,为Na2CO3溶液。
猜想(3):该溶液部分变质,为NaOH和Na2CO3的混合溶液。
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
| 实验操作 |
可能出现的现象与结论 |
同学评价 |
|
| 第1组 |
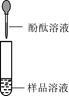 |
若溶液变红,则猜想(2)不成立 |
第2组同学认为:此方案结论不正确,理由是: 。 |
| 第2组 |
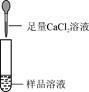 |
若产生白色沉淀,反应方程式是: ,则猜想(1)不成立。 |
第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立。 |
| 第3组 |
第一步第二步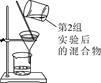 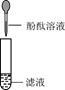 |
若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立。 |
第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是: |
【探究实验】综合各小组的方案后,动手实验。
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存。
【拓展延伸】同学们设计了下列两套装置进行实验: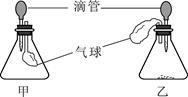
用胶头滴管吸取某种液体,锥形瓶中充入
一种气体或放入一种固体物质,挤压胶头滴管。
一段时间后,两装置中气球明显胀大。
(1)甲装置中可能发生反应的方程式是 。
(2)若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是 。