已知氧化性Fe3+>Cu2+。现将铜粉放入稀盐酸中,微热后无明显现象发生;当加入下列物质后,铜粉的质量减少。则加入的物质不可能是
| A.FeSO4 | B.Fe2(SO4)3 | C.KNO3 | D.HNO3 |
下列各物质制取反应原理中,符合绿色化理念,原子利用率最高的是
| A.实验室用铜和浓硫酸反应制取硫酸铜 |
| B.实验室用铜和稀硝酸反应制取一氧化氮 |
| C.工业上利用乙烯与水的加成反应制取乙醇 |
| D.工业上用焦炭还原三氧化二铁制取铁 |
下图为某兴趣小组制作的番茄电池,下列说法正确的是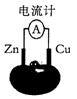
| A.电子由锌通过导线流向铜 | B.该装置将电能转化为化学能 |
| C.锌电极发生还原反应 | D.铜电极上无气泡产生 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.在标准状况下,22.4 L H2中含有氢原子数为2NA。 |
| B.常温常压下,23 g Na变为Na2O时失去的电子数为2NA。 |
| C.标准状况下,22.4 L CHCl3中含有的分子数为NA。 |
| D.常温常压下,l mol/L NaCl溶液中含有的钠离子数为NA。 |
可逆反应在一定条件下达到反应限度(化学平衡状态)的标志是
| A.反应停止了 | B.正反应速率与逆反应速率均为零 |
| C.反应物和生成物浓度相等 | D.正反应速率与逆反应速率相等 |
在下列三个反应中,过氧化氢(H2O2)所起的作用是
①H2O2+H2S===2H2O+S↓②2H2O2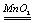 2H2O+O2↑③H2O2+C12==2HCl+O2↑
2H2O+O2↑③H2O2+C12==2HCl+O2↑
| A.均是氧化剂 | B.均是还原剂 |
| C.均既是氧化剂又是还原剂 | D.三个反应中所起作用各有不同 |