某甲酸溶液中含有甲醛,用下列方法可以证明的是
| A.加入足量的新制氢氧化铜并加热煮沸,有砖红色的沉淀 |
| B.加入过量的氢氧化钠充分反应后的溶液能发生银镜反应 |
| C.将试液进行酯化反应后的混合液能发生银镜反应 |
| D.加入足量氢氧化钠后,蒸馏出的气体通入新制的氢氧化铜悬浊液加热有砖红色沉淀 |
下列电离方程式书写不正确的是()
A.2H2O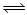 H3O++OH— H3O++OH— |
B.H2S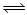 H++HS— H++HS— |
C.NaHS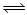 Na++HS— Na++HS— |
D.HCO3—+H2O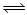 H3O++CO32- H3O++CO32- |
下列有关电池的说法不正确的是()
| A.手机上用的锂离子电池属于二次电池 | B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 | D.锌锰干电池中,锌电极是负极 |
下列有关实验基本操作和实验现象的描述正确的是()
| A.用托盘天平称取25.20 g氯化钠 |
| B.配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量 |
| C.用玻璃棒蘸取溶液滴到湿润的pH试纸上,测其pH |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
反应C(s)+H2O(g)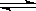 CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是
CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是
| A.增加固体C的量 | B.加入适当的催化剂 |
| C.保持压强不变,充入惰性气体使容器容积增大 | |
| D.保持容器容积不变,充入惰性气体使体系压强增大 |
运用元素周期律来判断,则下列叙述中不正确的是
| A.As是第4周期第ⅤA 族元素,则AsH3比NH3更稳定 |
| B.At是第6周期第ⅦA族元素,HAt不稳定,且AgAt是有色难溶于水的物质 |
| C.Sr是第4周期第ⅡA族元素,则SrSO4可能难溶于水,Sr(OH)2为强碱 |
| D.元素Be的金属性比Na的金属性弱 |