已知1~18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2—>Z — |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是(双选)( )
| A.可用铁做阳极材料 |
| B.电解过程中阳极附近溶液的pH升高 |
| C.阳极反应方程式为:2Cl-===Cl2+2e- |
| D.1 mol 二价镍全部转化为三价镍时,外电路中通过了1 mol 电子 |
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下图所示,电解总反应为:2Cu+H2O Cu2O+H2↑。下列说法正确的是( )
Cu2O+H2↑。下列说法正确的是( )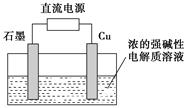
| A.石墨电极上产生氢气 |
| B.铜电极发生还原反应 |
| C.铜电极接直流电源的负极 |
| D.当有0.1 mol电子转移时,有0.1 mol Cu2O生成 |
下列描述中,不符合生产实际的是( )
| A.电解熔融的氧化铝制取金属铝,用铁做阳极 |
| B.电解法精炼粗铜,用纯铜做阴极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网做阴极 |
| D.在镀件上电镀锌,用锌做阳极 |
向三份0.1 mol·L-1CH3COONa溶液中分别加入少量NH4NO3、Na2SO3、FeCl3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
| A.减小、增大、减小 | B.增大、减小、减小 |
| C.减小、增大、增大 | D.增大、减小、增大 |
下列各组的比值等于2∶1的是( )
| A.pH均为12的烧碱溶液与氢氧化钡溶液的物质的量浓度之比 |
| B.硫化钾溶液中c(K+)与c(S2-)之比 |
| C.相同温度下0.2 mol·L-1醋酸溶液与0.1 mol·L-1醋酸溶液中c(H+)之比 |
| D.10 mL 0.5 mol·L-1的盐酸与5 mL 0.5 mol·L-1的盐酸中的c(H+)之比 |