某强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32―、SO32―、SO42―、C1―、NO2-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:
下列结论正确的是
| A.X中肯定存在Na+、Fe2+、A13+、NH4+、SO42― |
| B.气体F经催化氧化可直接生成气体D |
| C.沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3 、沉淀I一定是Al(OH )3 |
| D.X中不能确定的离子是 A13+、Na+、K+和C1― |
纳米材料是由纳米粒子(粒子直径 1 nm ~100nm)所组成的材料,它具有奇特的光、热、声、电、磁、力学和化学活泼性等理化性质.下列分散系中不含纳米粒子的是()
| A.无尘无雾含水蒸气的空气 | B.豆浆 |
| C.血液 | D.有色玻璃 |
下列反应中,浓硫酸表现出强氧化性的是()
①用铁槽车盛装浓硫酸 ②铜片与浓硫酸共热制备SO2
③浓硫酸与碘化钠固体共热 ④浓硫酸吸收NH3
⑤浓硫酸使蔗糖炭化时有刺激性气体产生
⑥将含水蒸气的氯气通过盛浓硫酸的洗气瓶
⑦浓硫酸和乙醇共热制乙烯 ⑧浓硫酸,乙醇和乙酸共热制乙酸乙酯
| A.⑤⑥⑦⑧ | B.①②⑤ | C.①②③⑤ | D.②③⑤ |
已知反应:①101 kPa时,2C(s)+O2(g) 2CO(g);ΔH = -221 kJ·mol—1②稀溶液中,H+(aq)+
2CO(g);ΔH = -221 kJ·mol—1②稀溶液中,H+(aq)+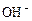 (aq)
(aq) H2O(l);ΔH = -57.3 kJ·mol—1。下列结论正确的是()
H2O(l);ΔH = -57.3 kJ·mol—1。下列结论正确的是()
| A.碳的燃烧热ΔH < -110.5 kJ·mol—1 |
| B.浓H2SO4和NaOH溶液反应生成1 mol水时放出57.3 kJ的热量 |
| C.稀硫酸与稀NaOH溶液反应的中和热ΔH =" +57.3" kJ·mol—1 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水时放出57.3 kJ热量 |
下列实验一定能证明有SO2存在的是()
①能使澄清石灰水变浑浊 ②能使蓝色石蕊试纸变红色 ③能使品红溶液褪色 ④通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成 ⑤先通入足量的NaOH溶液,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸
| A.都能证明 | B.都不能证明 | C.③④⑤ | D.④ |
一定能在下列溶液中大量共存的离子组是()
A.含有大量Al3+的溶液:Na+、 、 、 、 、 |
B.c(H+) = 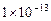 mol·L—1的溶液:Na+、Ca2+、 mol·L—1的溶液:Na+、Ca2+、 、 、 |
C.含有大量Fe3+的溶液:Na+、Mg2+、 、 、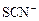 |
D.含有大量 的溶液:H+、Fe2+、 的溶液:H+、Fe2+、 、 、 |