常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-), 根据图示判断,下列说法正确的是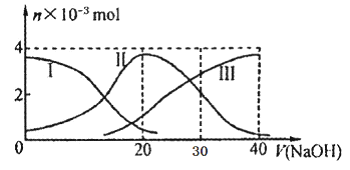
A.H2A在水中的电离方程式是: H2A === H+ + HA- ; HA-  H+ + A2-
H+ + A2-
B.当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D. 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+ c(HA-)+ 2c(H2A)= c(A2-)+ 2 c(OH-)
将土豆切开后,一段时间后可观察到切面变蓝,说明土豆中含有
| A.淀粉和I- | B.淀粉和I2 |
| C.淀粉和KIO3 | D.葡萄糖和I2 |
下列为人体提供能量的营养物质中,属于高分子化合物的是
| A.油脂 | B.蔗糖 | C.蛋白质 | D.葡萄糖 |
你认为减少酸雨不可采用的措施是
| A.煤脱硫再作燃料 | B.开发新能源 |
| C.把工厂烟囱升高 | D.多用风能、氢能、核能等 |
向Fe2O3、CuO、Fe、Cu的混和粉末中加入过量的稀硫酸,充分反应后,仍有红色粉末存在,则关于溶液中阳离子的判断正确的是
| A.只有Fe2+和Cu2+ |
| B.一定有Fe2+、Cu2+,可能有Fe3+ |
| C.一定有Fe2+,可能有Cu2+ |
| D.只有Fe2+ |
为了防止FeSO4被氧化而变质,实验室在配制FeSO4溶液时,常在溶液中加入少量的
| A.铜粉 | B.铁粉 | C.锌粉 | D.Fe2(SO4) |