下列物质中,在常温常压时呈气态的是( )
| A.乙炔 | B.苯 | C.乙醇 | D.四氯化碳 |
pH=4的醋酸和氯化铵溶液中,水的电离程度的关系前者与后者比较()
| A.大于 | B.小于 | C.等于 | D.无法确定 |
下列各式中属于正确的水解反应离子方程式的是()
A.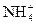 +H2O +H2O NH3·H2O+H+ NH3·H2O+H+ |
B.S2-+2H2O H2S+2OH- H2S+2OH- |
C.CH3COOH+H2O CH3COO-+H3O+ CH3COO-+H3O+ |
D.CH3COOH+OH-====CH3COO-+H2O |
能证明醋酸是弱酸的事实是()
| A.醋酸能使紫色石蕊试液变红 |
| B.醋酸能被弱碱氨水中和 |
| C.醋酸钠溶液的pH大于7 |
| D.常温下,0.1mol·L-1醋酸溶液中的c(H+)为1.32×10-3mol·L-1 |
为了除去氯化镁酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量的盐酸,这种试剂是()
| A.MgCO3 | B.NH3·H2O | C.Na2CO3 | D.NaOH |
用物质的量都是0.1mol的HCN和NaCN配成1L混合溶液,已知其中c(CN-)小于c(Na+),则下列判断正确的是()
| A.c(H+)>c(OH-) | B.c(HCN)+c(CN-)=0.2mol·L-1 |
| C.c(Na+)>c(CN-)>c(H+)>c(OH-) | D.c(CN-)>c(OH-)=0.1mol·L-1 |