向某晶体的溶液中加入含Fe2+的溶液无明显变化,当滴加几滴溴水后,混合液出现红色,由此得出下列的结论错误的是( )。
| A.Fe3+的氧化性比溴的氧化性强 |
| B.该晶体中一定含有SCN- |
| C.Fe2+与SCN-不能形成红色化合物 |
| D.Fe2+被溴氧化成Fe3+ |
下列金属中,通常采用热还原法冶炼的是
| A.Na | B.Al | C.Fe | D.Ag |
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,1.6 g臭氧中含有6.02×1022个氧原子 |
| B.标准状况下,2.24 L水中含有6.02×1022个水分子 |
| C.2.24 L氨气分子中含6.02×1023个电子 |
| D.2.4 g金属镁变为镁离子时失去6.02×1022个电子 |
如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是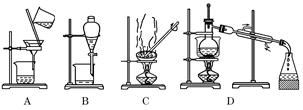
下列物质中,属于天然有机高分子化合物的是
| A.葡萄糖 | B.蔗糖 | C.油脂 | D.淀粉 |
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
…… |
| C2 H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
…… |
A.C6H12 B.C6H14 C.C7H12 D.C7H14