将含有0.1 mol SiO2的铝、硅混合物分别与足量NaOH溶液、盐酸混合,充分反应后前者可得到11.2 L气体(标准状况),后者可得到6.72 L气体(标准状况),则参加反应的n(HCl)与n(NaOH)之比为( )。
| A.1∶1 | B.1∶2 | C.2∶1 | D.3∶1 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是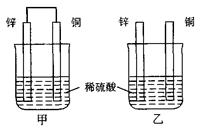
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.产生气泡的速度甲比乙快 |
下列各组物质的性质依次递减的是
| A.碱性:Al(OH)3、Mg(OH)2、NaOH |
| B.还原性:HI、HBr、HCl |
| C.酸性:HClO4、H2SO4、H3PO4 |
| D.稳定性:H2CO3、NaHCO3、Na2CO3 |
能表明非金属甲的非金属性比非金属乙的非金属性强的叙述正确的是:
| A.在氧化还原反应中,甲得电子比乙得电子多 |
| B.甲的最高价氧化物对应水化物酸性比乙的的最高价氧化物对应水化物酸性强 |
| C.甲的氢化物水溶液酸性比乙的氢化物水溶液酸性强 |
| D.向含甲和乙的阴离子的钠盐混合溶液中通入氯气,乙的阴离子先反应 |
工业上用来贮存和运输浓硫酸、浓硝酸的容器能用以下( )材料制造的。
| A.玻璃 | B.铝 | C.铁 | D.铜 |
绿色化学提倡化工生产应提高原子利用率,原子利用率表示目标产物的质量与生成物总质量之比。在下列制备环氧乙烷的反应中,原子利用率最高的是()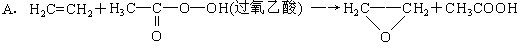
B.CH2=CH2+Cl2+Ca(OH)2 
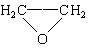 +CaCl2+H2O
+CaCl2+H2O
C.2CH2=CH2+O2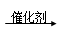
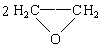
D.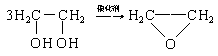 +HOCH2CH2-O-CH2CH2OH+2 H2O
+HOCH2CH2-O-CH2CH2OH+2 H2O