高温下,某反应达平衡,平衡常数K=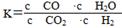 ,恒容时,温度升高,H2浓度减小。下列说法正确的是( )
,恒容时,温度升高,H2浓度减小。下列说法正确的是( )
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO+H2O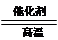 CO2+H2 CO2+H2 |
下列溶液中Cl-的物质的量浓度最小的是
| A.200mL 2mol/L MgCl2溶液 | B.1000mL 2.5mol/L NaCl溶液 |
| C.250mL 1mol/L AlCl3溶液 | D.300mL 5mol/L KClO3溶液 |
在Na2SO4、NaCl、NaOH的混合溶液中,Na+、SO42-、OH-的个数比是8:1:2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比是
| A.1:1:1 | B.1:4:2 | C.1:2:4 | D.1:3:2 |
用下图表示的一些物质或概念间的从属关系中不正确的是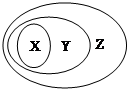
| X |
Y |
Z |
|
| A |
氧化物 |
化合物 |
纯净物 |
| B |
胶体 |
分散系 |
混合物 |
| C |
电解质 |
酸、碱、盐 |
化合物 |
| D |
碱性氧化物 |
金属氧化物 |
氧化物 |
标准状况下有①6.72LCH4②3.01×1023个HCl ③13.6gH2S ④0.2molNH3,下列对四种气体的关系从小到大表示不正确的是
| A.体积 ④<①<③<② | B.密度 ①<④<③<② |
| C.质量 ④<①<③<② | D.氢原子数 ④<②<③<① |
在200mL某硫酸盐溶液中,含硫酸根离子1.5NA个,含金属离子NA个,则该硫酸盐溶液的物质的量浓度为
| A.2.5mol/L | B.5mol/L | C.7.5mol/L | D.2mol/L |