某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)乙同学认为甲同学的结论是错误的,他的理由是 (用化学方程式表示),所以他认为应该检验 (填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。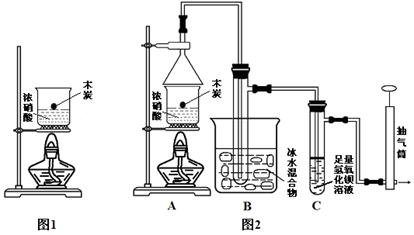
(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号) 。
①将炭与浓硝酸一同放在装置中加热;②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸; ④先加热炭,再将炭投入冷浓硝酸。
(3)请用平衡移动原理解释B装置的作用 。
(4)C装置中出现的现象是 ,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式 。
| A.银镜反应实验后附有银的试管,可用稀H2SO4清洗 |
| B.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次 |
| C.不慎将浓硫酸沾在皮肤上,立即用NaOH溶液冲洗 |
| D.配制FeCl3溶液时,将FeCl3固体溶于较浓盐酸中,然后再用水稀释到所需的浓度 |
E.用10mL的量筒量取4.80mL的浓硫酸
F.不慎接触过多的氨,及时吸人新鲜的空气和水蒸气,并用大量水冲洗眼睛
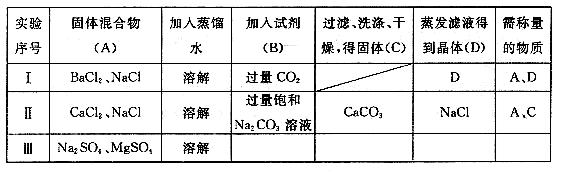
试回答下列问题:
(1)实验Ⅰ中D 的成分是___________称量后_________(填“能”或“不能”)通过计算得到A中各组分的质量比.
(2)实验II 填写的内容中明显错误的是________,其原因________________________
(3)对实验Ⅲ进行设计,并将相应内容填入Ⅲ中对应的空格内,最终能得出A中各组分的质量比为:(用含字母的表达式表示)____________________________
要除去表中所列有机物中的少量杂质(括号内为杂质),从(Ⅰ)中选择适宜的试剂,从(Ⅱ)中选择分离提纯的方法,用序号填入表中。
(Ⅰ)试剂:a.NaCl固体;b.NaOH溶液;c.生石灰;d.Na2CO3溶液;e.水;f.浓溴水;g.KMnO4溶液
(Ⅱ)方法:
| A.过滤; | B.萃取; | C.蒸馏; | D.分液;E.盐析;F.重结晶 |
| 要提纯物质(杂质) |
CH3CH2Br(CH3CH2OH) |
C2H5OH(H2O) |
肥皂液(甘油) |
C6H5Br(Br2) |
C6H6(C6H5OH) |
| 选用试剂(Ⅰ) |
|||||
| 分离方法(Ⅱ) |
将下图所列仪器组装为一套实验室蒸馏石油的装置,并进行蒸馏,得到汽油和煤油。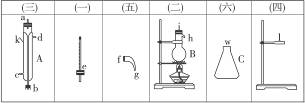
(1)图中A、B、C三种仪器的名称是____________________________________________。
(2)将以上仪器按(一) (六)顺序,用字母a,b,c…表示连接顺序:
(六)顺序,用字母a,b,c…表示连接顺序:
e接_________,_________接_________,_________接_________,_________接_________。
(3)A仪器中c口是_________,d口是_________(填“进水口”或“出水口”)。
(4)蒸馏时,温度计水银球应在_________位置。
(5)在B中注入原油后,加几片碎瓷片的目的是___________________________。
(6)给B加热,收集到沸点60—150 ℃间的馏分是_________,收集到150—300 ℃间的馏分是_________。
下图中A~D是中学化学实验中常见的几种温度计装置示意图。
(1)请从①~⑧中选出必须使用温度计的实验,把编号填入最适宜的装置图A~C下的空格中。
①酒精和浓硫酸混合加热制乙烯 ②电石跟水反应制乙炔 ③分离苯和硝基苯的混合物 ④苯与溴的取代反应 ⑤石油的分馏 ⑥浓盐酸与二氧化锰混合加热制氯气 ⑦测定硝酸钾在水中的溶解度 ⑧食盐和浓硫酸混合加热制氯化氢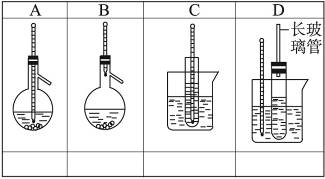
(2)选用D装置做苯的硝化实验,D中长玻璃管的作用是___________________________。