电解原理在化学工业中有着广泛的应用。图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。则下列说法不正确的是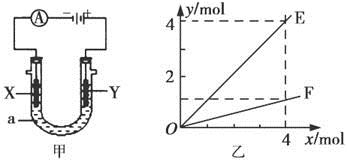
| A.若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 |
| B.按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 |
| C.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol |
| D.若X、Y为铂电极,a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol·L-1 |
氢化锂(LiH)属于离子化合物。LiH跟水反应可以放出氢气。下列叙述中正确的是
| A.LiH的水溶液显中性 | B.LiH中的氢离子可以被还原生成氢气 |
| C.LiH是一种强氧化剂 | D.LiH中氢离子比锂离子的半径大 |
下列离子在指定条件下能大量共存的是
| A.在酸性溶液中:Ba2+、K+、SO42―、Cl― |
| B.含有大量Al3+的溶液中:K+、Na+、NH4+、SO42― |
| C.使甲基橙变黄的溶液中:Na+、I―、CO32―、OH― |
| D.无色溶液中:K+、Cl―、Cr2O72-、HCO3― |
下列实验“实验操作”与“结论”对应关系正确的是
| 选项 |
实验操作 |
结论 |
| A |
向Fe(NO3)2溶液的试管中加入稀H2SO4 ,在管口观察到红棕色气体 |
HNO3分解生成了NO2 |
| B |
向沸水中逐滴加入1~2 mL FeCl3饱和溶液,煮沸至红褐色液体 |
制备Fe(OH)3胶体 |
| C |
常温下,向饱和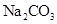 溶液中加少量 溶液中加少量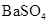 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 |
说明常温下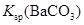 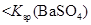 |
| D |
向纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
元素及其化合物丰富了物质世界,下列说法正确的是
| A.铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象 |
| B.NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| C.金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D.Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应 |
下列有关铜锌原电池(下图)的叙述正确的是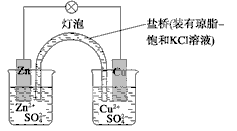
| A.正极反应为Zn-2e-===Zn2+ | B.取下盐桥,原电池仍可工作 |
| C.在外电路中,电子从正极流向负极 | D.电池反应为Zn+Cu2+===Zn2++Cu |