已知常温下CH3COOH的电离平衡常数为Ka。常温下,向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是
| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol·L-1 |
| B.b点表示的溶液中c(CH3COO-)>c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中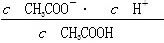 相等 相等 |
由配位键形成的离子[Pt(NH3)6]2+和[PtCl4]2—中,两个中心离子铂的化合价是()
| A.都是+8 | B.都是+6 | C.都是+4 | D.都是+2 |
离子晶体之所以有脆性是由于()
| A.离子排列不能错位 | B.离子键结合力大 |
| C.离子键有方向性 | D.离子键有饱和性 |
下列各组物质中,化学键的类型(离子键、共价键)相同的是()
| A.CO和MgCl2 | B.NH4F和NaF |
| C.Na2O2和H2O2 | D.H2O和SO2 |
下列物质中,含有非极性共价键的离子化合物是()
| A.Na2O2 | B.NaOH | C.H2O2 | D.NH3·H2O |
下面几种离子化合物中,离子键极性最强的是()
| A.KCl | B.NaCl | C.AlCl3 | D.Na2S |