向20 mL 0.5 mol·L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中错误的是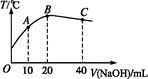
| A.醋酸的电离平衡常数:B点>A点 |
| B.由水电离出的c(OH-):B点>C点 |
| C.从A点到B点,混合溶液中可能存在:c(CH3COO-)=c(Na+) |
| D.从B点到C点,混合溶液中一直存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
在盛放酒精的试剂瓶的标签上应印有下列警示标记中的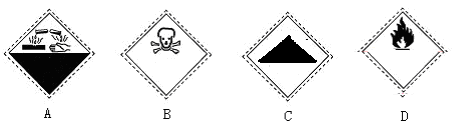
设NA表示阿伏加德罗常数,下列叙述正确的是
| A.常温下,23g NO2含有NA个氧原子 |
| B.25℃、101kPa时,11.2L H2中含有的原子数为NA |
| C.标准状况下,22.4LCCl4中含有的分子数为NA |
| D.2.3g的金属钠与足量的水反应时失去的电子数为0.1NA |
下列是某同学对相应反应的离子方程式所作的评价,其中对应的评价合理的是
| 编号 |
化学反应 |
离子方程式 |
评价 |
| A |
把MgSO4溶液滴入Ba(OH)2溶液 |
Mg2++2OH-=Mg(OH)2↓ |
正确 |
| B |
氧化铜与稀盐酸反应 |
CuO+2H+══Cu2++H2O |
正确 |
| C |
向FeCl2溶液中通入氯气 |
Fe2++Cl2=Fe3++2Cl- |
错误,电荷不守恒 |
| D |
AlCl3溶液中加足量氨水 |
Al3++ 3OH- ══ Al(OH)3↓ |
正确 |
在6KOH + 3Cl2 ="=" KClO3 + 5KCl + 3H2O的反应中,下列说法中正确的是
| A.KCl是还原产物,KClO3是氧化产物 |
| B.KOH是氧化剂,Cl2是还原剂 |
| C.Cl2是既是氧化剂,又是还原剂 |
| D.被氧化的氯原子与被还原的氯原子数之比为1∶5 |
下列方法正确的是
| A.容量瓶使用前要先检查是否漏液 |
| B.液态HCl、固体NaCl均不导电,但HCl、NaCl是电解质 |
| C.钠在空气中长时间放置,最终变为NaOH |
| D.物质的量相等的Na2CO3、NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多 |