常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是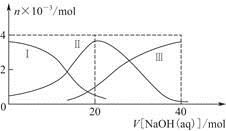
| A.当V[NaOH(aq)]=20 mL时,溶液中离子浓度大小关系: c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 |
| C.H2A第一步电离的方程式为H2A=HA-+H+ |
| D.向NaHA溶液加入水稀释的过程中,pH可能增大也可能减小 |
金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石。已知12 g石墨完全转化为金刚石时,要吸收E kJ的能量,下列说法正确的是( )
| A.金刚石与石墨互为同位素 |
| B.石墨不如金刚石稳定 |
| C.金刚石不如石墨稳定 |
| D.等质量的石墨与金刚石完全燃烧,石墨放出的能量多 |
对化学反应限度的叙述,错误的是( )
| A.任何可逆反应都有一定的限度 |
| B.化学反应达到限度时,正逆反应速率相等 |
| C.化学反应的限度与时间的长短无关 |
| D.化学反应的限度是不可改变的 |
下列说法正确的是( )
| A.物质发生化学反应时都伴随着能量变化 |
| B.伴有能量变化的物质变化都是化学变化 |
| C.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
| D.放热反应的发生无需任何条件 |
把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化如下图所示。在下列因素中,影响反应速率的因素是()
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
| A.①④ | B.③④ | C.①②③ | D.②③ |
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1 mol氢气中的化学键吸收的能量为Q1 kJ,破坏1 mol氯气中的化学键吸收的能量为Q2 kJ,形成1 mol氯化氢中的化学键释放的能量为Q3 kJ。下列关系式中,正确的是()
| A.Q1+Q2>Q3 | B.Q1+Q2>2Q3 | C.Q1+Q2<Q3 | D.Q1+Q2<2Q3 |