向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)  SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
同温同压下,等质量的下列气体所占有的体积最大的是( )
| A.O2 | B.CH4 | C.CO2 | D.SO2 |
为了萃取碘水中的碘,不能选用的萃取剂是( )
| A.CCl4 | B.酒精 | C.汽油 | D.苯 |
如图所示,容量瓶的刻度线标在比较细的瓶颈之上。以下是某同学猜测关于这样做的原因,你认为正确的是 ( )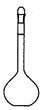
| A.为了美观 | B.为了统一标准 | C.为了提高准确度 | D.方便刻画 |
下列实验操作中,不合理的是( )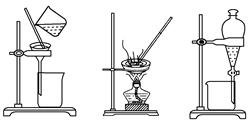
①②③
| A.洗涤沉淀时(如图①),向漏斗中加适量水,搅拌并滤干 |
| B.用CCl4提取碘水中的碘,选③ |
| C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干 |
| D.粗盐提纯,选①和② |
如果你家里的食用花生油混有水份,你将采用下列何种方法分离( )
| A.过滤 | B.蒸馏 | C.分液 | D.萃取 |