设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
| T/K |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1 173 |
2.15 |
1.67 |
下列有关叙述正确的是( )
A.b<0
B.在973 K下增大压强,K2增大
C.a>b
D.在常温下反应①一定能自发进行
下列关于二氧化硫的说法,正确的是
| A.能漂白某些物质,说明其有氧化性 |
| B.能使紫色石蕊试液变红,说明其水溶液呈酸性 |
| C.能用浓硫酸干燥,说明其不具有还原性 |
| D.能使溴水腿色,说明其具有漂白性 |
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是
| A.甲是浓氨水,乙是浓硫酸 |
| B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 |
| D.甲是浓硝酸,乙是浓氨水 |
下列实验装置图所示的实验操作,不能达到相应实验目的的是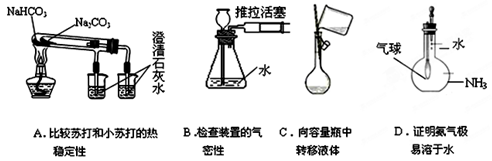
用铁片与稀硫酸反应时,下列措施不能使反应速率加快的是
| A.加热 | B.不用铁片,改用铁粉 |
| C.滴加少量的CuSO4溶液 | D.不用稀硫酸,改用98%浓硫酸 |
下列各图所表示的反应是吸热反应的是
A、 B 、 C 、 D、