下列有关电池的说法不正确的是( )
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
桶烯(Barrelene)结构简式如下图所示,有关说法不正确的是
| A.桶烯分子中所有原子不可能在同一平面内 |
| B.桶烯在一定条件下能发生加成反应 |
| C.桶烯的分子式C8H8 |
| D.桶烯的一个氢原子被氯原子取代,有四种结构 |
如果定义有机物的同系列是一系列结构式符合 (其中n=0、1、2、3……)的化合物。式中A、B是任意一种基团(或氢原子),W为2价的有机基团,又称为该同系列的系差。同系列化合物的性质往往呈现规律性变化。下列四组化合物中,不可称为同系列的是
(其中n=0、1、2、3……)的化合物。式中A、B是任意一种基团(或氢原子),W为2价的有机基团,又称为该同系列的系差。同系列化合物的性质往往呈现规律性变化。下列四组化合物中,不可称为同系列的是
A.CH3CH2CH2CH3 CH3CH2CH2CH2CH3 CH3CH2CH2CH2CH2CH3
B.CH3CH=CHCHO CH3CH=CHCH=CHCHO CH3(CH=CH)3CHO
C.CH3CH2CH3 CH3CHClCH2CH3 CH3CHClCH2CHClCH3
D.ClCH2CHClCCl3 ClCH2CHClCH2CHClCCl3ClCH2CHClCH2CHClCH2CHClCCl3
近年来用合成方法制备了多种新奇的有机物,例如分子具有如下图所示立体结构的环状化合物: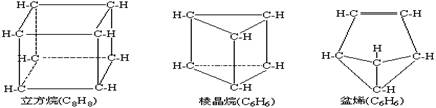
有人认为上述有机物中①立方烷、棱晶烷可以看做是烷烃的同系物;②盆烯是乙烯的同系物;③棱晶烷、盆烯是苯的同分异构体。上述看法中正确的是
| A.②③ | B.除①都正确 | C.只有① | D.只有③ |
已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如下图:则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为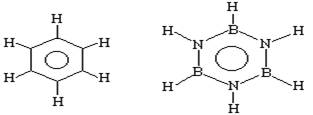
| A.2种 | B.3种 | C.4种 | D.6种 |
利用某些有机物之间的相互转换可以贮存太阳能,如原降冰片二烯(NBD)经过太阳光照转化成为四环烷(Q)的反应为如下所示,以下叙述不正确的是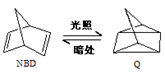
A.NBD的能量比Q的能量低
B.NBD和Q互为同分异构体
C.NBD能发生加成反应而Q不能
D.NBD不能使酸性KMnO4溶液褪色而Q能