在25 ℃、101 kPa时,CH4(g)、H2(g)、C(s)的燃烧热分别是-890.3 kJ·mol-1、-285.8 kJ·mol-1和-393.5 kJ·mol-1,则CH4(g)—→C(s)+2H2(g)的ΔH是
| A.-74.8 kJ·mol-1 | B.+74.8 kJ·mol-1 |
| C.-211.0 kJ·mol-1 | D.+211.0 kJ·mol-1 |
下列实验操作能达到目的的是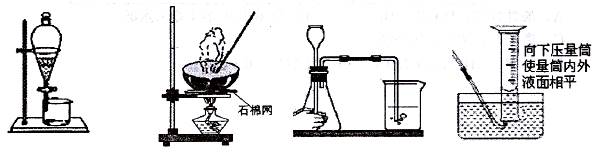
| A.分离碘酒中的碘 | B.蒸发 | C.检查装置气密性 | D.读取气体体积 |
下列广告语对应商品中含有的物质有误的是
| A.“红梅味精,领先(鲜)一步”--蛋白质 |
| B.“衡水老白干,喝出男人味”——乙醇 |
| C.“吃了钙中钙,腰不疼了,腿不痛了,腰杆也直了”——碳酸钙 |
| D.“要想皮肤好,早晚用大宝”——丙三醇 |
人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”。在“五金”顺序中,把一种金属的位置向后移一位,正好符合某化学规律。这种金属和该化学规律是
| A.铁、金属活动性顺序表 | B.金、质量守恒定律 |
| C.银、元素周期律 | D.铜、金属密度顺序表 |
将1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入浓度为1.0 mol·L-1的 NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀,下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是16∶3 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.反应中转移电子的物质的量为0.06 mol |
向稀硫酸中加入铜粉不发生反应,若再加入某种盐,则铜粉可以逐渐溶解,该盐是
| A.KNO3 | B.ZnSO4 | C.KCl | D.FeSO4 |