一包白色粉末,由几种常见的盐混合组成,其中只可能含有Na+、K+、Al3+、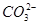 、
、 、
、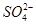 、
、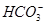 、
、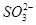 中的若干种离子。某同学对该溶液进行如下实验:
中的若干种离子。某同学对该溶液进行如下实验: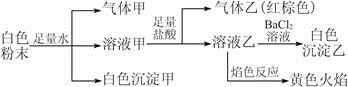
以下说法正确的是
A.白色沉淀甲是Al(OH)3,气体甲是CO2,所以混合物一定含Al3+和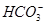 |
| B.气体乙一定是NO和NO2的混合气体 |
C.白色沉淀乙是BaSO4,所以原混合物一定含有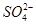 |
| D.焰色反应为黄色火焰,不能确定原混合物中不含K+ |
右图模拟"侯氏制碱法"制取 的部分装置。下列操作正确的是()
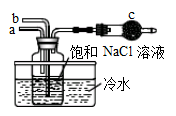
| A. | 通入 ,然后 通入 , 中放碱石灰 |
| B. | 通入 ,然后 通入 , 中放碱石灰 |
| C. | 通入 ,然后 通入 , 中放蘸稀硫酸的脱脂棉 |
| D. | 通入 ,然后 通入 , 中放蘸稀硫酸的脱脂棉 |
只改变一个影响因素,平衡常数 与化学平衡移动的关系叙述错误的是
| A. | 值不变,平衡可能移动 | B. | 值变化,平衡一定移动 |
| C. | 平衡移动, 值可能不变 | D. | 平衡移动, 值一定变化 |
催化加氢可生成 3-甲基己烷的是()
| A. | B. | ||
| C. | D. |
如右图所示,将铁棒和石墨棒插入盛有饱和
溶液的
型管中。下列分析正确的是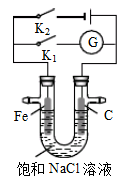
| A. | 闭合,铁棒上发生的反应为2 |
| B. | 闭合,石墨棒周围溶液 逐渐升高 |
| C. | 闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D. | 闭合,电路中通过0.002 个电子时,两极共产生0.001 气体 |
向饱和澄清石灰水中加入少量 ,充分反应后恢复到原来的温度,所得溶液中()
| A. | 、 均增大 | B. | 、 均保持不变 |
| C. | 、 均减小 | D. | 增大、 减小 |