已知X、Y、Z、W均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物已略)。下列说法不正确的是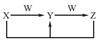
| A.X、Y、Z中至少有一种相同的元素,该元素可以是金属元素也可以是非金属元素 |
| B.物质W可能是化合物,也可能是单质 |
| C.上述转化关系中不可能出现置换反应 |
| D.若X、Y、Z中均含有一种常见金属元素,则W可能是强酸也可能是强碱 |
下列说法正确的是()
| A.金属氧化物都是碱性氧化物 | B.盐电离出的离子不一定有金属离子 |
| C.由同种元素组成的物质一定是单质 | D.非金属氧化物都是酸性氧化物 |
有含碳元素的质量分数相同的A、B两种烃,关于A和B的叙述中正确的是
A.二者不可能是同系物
B.二者一定是同分异构体
C.各1mol的A和B分别燃烧生成CO2的质量一定相等
D.二者最简式相同
肉桂醛是一种食用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中。工业上可通过下列反应制备: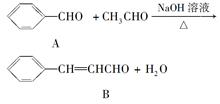
下列相关叙述正确的是
①B的相对分子质量比A大28 ②A、B可用于酸性高锰酸钾溶液鉴别
③B中含有的含氧官能团是醛基、碳碳双键 ④A、B都能发生加成反应、还原反应
⑤A能发生银镜反应 ⑥B的同类同分异构体(含苯环、包括B)共有5种
⑦A中所有原子一定处于同一平面
A.①②⑤B.③④⑤ C.④⑤⑥D.②⑤⑥⑦
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是
| A.乙烯能发生加成反应,乙烷不能发生加成反应 |
| B.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 |
| C.甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 |
| D.苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 |
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有
| A.15种 | B.28种 | C.32种 | D.40种 |