金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)生铁和钢都是铁的合金,但是性质上有很大的差异,这是因为 ,钢铁制品在生活中用途广泛,但却易生锈,写出一种防止铁锅生锈的做法 。
(2)铝比铁活泼,但铝在空气重表现出良好的抗腐蚀性,为什么?
(3)为了探究X、Y、Z三种固体金属的活动性,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化,将X和Z浸入硝酸银溶液中X表面有银析出而Z无变化。根据以上事实回答:
①X、Y、Z三种金属的活动性由强到弱的顺序为
| A.X Y Z | B.Y X Z | C.Z X Y | D.X Z Y |
②写出金属X的化学式
(4)铜以及铜合金的应用有着悠久的历史。现有黄铜(铜、锌合金)20g,放入烧杯中,加入50g的稀盐酸,恰好完全反应,测得烧杯内剩余物质的质量为69.6g。请计算黄铜样品中锌的质量分数。
结合图示装置回答下列问题。
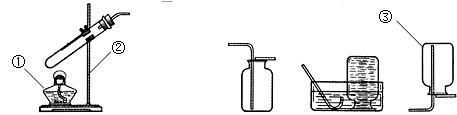 |
A B C D E
⑴写出标号仪器的名称:①_____________,②_____________,③_____________;
⑵实验室若用过氧化氢溶液和二氧化锰混合制取氧气,则你选用的发生装置是,如果要收集比较干燥的氧气,你会用收集。
⑶用高锰酸钾制取氧气的化学式表达式为①,若选择A和D装置制取并收集氧气,则要对A装置进行的改进是②,
③。实验结束时应先___________④___________再____________⑤__________,否则会导致____________⑥__________炸裂试管。
⑷常温下实验室可用金属锌粒和稀硫酸液体反应制取较纯净的氢气,则应选择的装置组合是________。
国庆期间小明同学去惠山旅游时,用瓶装了一些山下的泉水,带回实验室,在老师的指导下,按下列流程进行实验,制取蒸馏水。
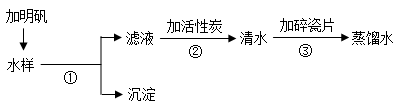 |
请回答下列问题:
⑴取水后加入明矾的作用是__________________________________________。
⑵操作①的名称是____________,操作③的名称是____________。
⑶操作②是加活性炭过滤,利用其_________性,除去水样中的色素和异味。
⑷要检验“清水”是硬水还是软水可取样品加入_________。制得的蒸馏水属于_________(填“硬水”或“软水”)。
⑸在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是_______________________。
元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题: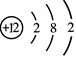
| IA |
0 |
||||||||
| 1 |
1 H 氢 1.008 |
2 He 氦 4.003 |
|||||||
| IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
||||
| 2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
| 3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
⑴请从上表中查出地壳中含量最多的金属元素的相对原子质量为。
⑵表中不同种元素最本质的区别是(填序号):
A.相对原子质量不同 B.质子数不同 C.中子数不同
⑶元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:(填字母序号)、……
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
⑷元素周期表中,原子序数为12的镁元素的原子结构示意图如右上图,该原子在化学反应中易(填“得到”或“失去”)电子。说明元素的化学性质与原子的
关系密切。
有A、B、C、D四种元素,A元素的原子没有中子;B元素的离子结构示意图如右图所示;C+的核外电子排布与氖原子相同,D元素的原子有三个电子层,第一层和第三层电子数的和比第二层电子数多1。 试回答:⑴A、D二种元素的名称或符号是:A_________、D_________;
试回答:⑴A、D二种元素的名称或符号是:A_________、D_________;
⑵B、C二种元素的离子符号:B_________、C_________;
⑶C、D二种元素组成化合物的化学式是_________。
右图为电解水的装置简图。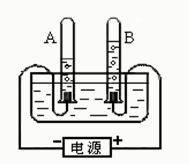
⑴通__________(填“直流电”或“交流电”)一段时间后
停止通电,试管A和试管B中所收集到的气体的体积比
约为____________。试管A中的气体是______;
⑵这个实验说明水是由_______________________组成的;
反应的化学式表达式是______________________________。