下表是元素周期表中的1~18号元素原子核外电子排布,我们对它进行研究: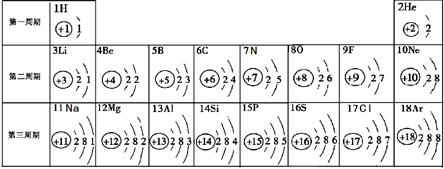
(1)从原子结构上分析,图中氧、硫元素具有相似化学性质的主要原因是 ;
(2)写出质子数为1、6、8、11四种元素组成的可以治疗胃酸过多物质的化学式: 。
(3)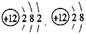 表示一种元素的两种粒子,它们属于同一种元素的依据是 。
表示一种元素的两种粒子,它们属于同一种元素的依据是 。
(4)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因 。
(6分)已知A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,其中A、C、D、M、F为氧化物,组成A与C的元素种类相同;H为可溶性碱;固体X在B中充分燃烧可生成无色气体D;E为常用建筑材料的主要成分。各物质之间的相互关系如下图所示(部分反应条件和生成物已省略(。
(1)物质A的化学式为:_________;
(2)写出G和N反应的化学方程式_____________________________;
(3)物质F的俗称为__________,它与C反应的现象为_____________;
(4)该转化过程中没有涉及到的基本反应类型为_______________。
(6分)下图是a、b、c三种物质(均不含结晶水(的溶解度曲线,请填空:
(1)点P表示的意义为______________________。
(2)将t3℃时a、b、c三种物质饱和溶液的温度降低到t1℃时,三种溶液的溶质质量分数大小关系是____________。
(3)在t2℃时将等质量的a、b、c三种物质分别放入一定量的水中恰好完全溶解,配制成饱和溶液,则所得溶液质量由大到小的顺序为________________。
(4)a、b、c三种物质中能通过升温将接近饱和的溶液变为饱和的是_______。
(5)在t3℃时取a物质50g配制成饱和溶液,若需要将该饱和溶液稀释为溶质质量分数为25%的溶液,需要加水的质量为_________。
(8分)完成化学反应方程式。
(1)铁丝在氧气中燃烧________________________________
(2)铜与硝酸银反应____________________________________
(3)在催化剂的作用下氯酸钾制氧气_______________________________
(4)盐酸除铁锈_______________________________
水是生命之源,也是日常生活、工农业生产必不可少的。
(1)清澈的温泉水是_____(填“纯净物”或“混合物”)。
(2)净化温泉水的过程中,活性炭的主要作用是。
(3)鉴别生活用水是硬水还是软水,方法是(写出操作过程、现象、结论)_____________。
(4)制备碳酸饮料时,水参与反应生成了碳酸,写出相关化学方程式____________。
(5)节约、保护水资源是每个人的责任,请列举一条生活中你的节水做法________。
铜在工农业生产中应用广泛。请回答:
(1)如图所示为某铜元素的所呈现的信息。则铜元素的质子数为______,相对原子质量为__________;
(2)铜单质可以作为导体的原因是__________;
(3)硫酸铜可以与消石灰按照一定比例配制波尔多液,试用化学方程式说明不能用铁制品盛放的原因________________;
(4)氢氧化铜不稳定,在加热的情况下易分解,生成一种黑色固体和水,试写出分解的化学方程式___________;