化学实验课上,某同学向含有稀硫酸的硫酸铜溶液中,逐滴滴入NaOH溶液至过量。记录滴入NaOH溶液质量(x)与有关量的变化关系如图所示(提示:硫酸铜溶液呈酸性),下列判断错误的是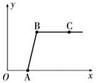
| A.图中纵坐标(y)表示生成Cu(OH) 2的质量 |
| B.反应进行到B点时,溶液中的溶质是Na2SO4 |
| C.AB段溶液的pH逐渐增大 |
| D.B点和C点溶液的pH相等 |
酚酞遇到下列物质不能变红的是()
| A.稀硫酸 | B.烧碱 | C.石灰水 | D.肥皂水 |
某同学探究金属单质的活泼性时发现:X、Y都能与稀硫酸反应放出氢气而Z不能;Y能在X的盐溶液中置换出X。则它们的金属活动顺序为 ()
| A.X>Y>(H)>Z | B.Y>X>(H)>Z | C.X>Z>(H)>Y | D.Y>(H)>X> Z |
实验室用高锰酸钾制取氧气时有如下操作步骤:①点燃酒精灯,②检查装置的气密性,③装药品,④用排水集气法收集,⑤把导气管撤离水面,⑥熄灭酒精灯,⑦把试管固定在铁架台上。其中操作顺序正确的是()
| A.②③⑦①④⑥⑤ | B.②③⑦①④⑤⑥ |
| C.⑤⑦③②①④⑥ | D.③①⑦②④⑥⑤ |
芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:SiO2 + 2C Si +2CO↑,该反应的基本类型是()
Si +2CO↑,该反应的基本类型是()
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
能使硝酸钾饱和溶液变成不饱和溶液的正确措施是()
| A.降低温度 | B.加入水 | C.加入硝酸钾 | D.增大压强 |