下列各组物质的性质比较,正确的是
| A.酸性:HClO4>H3PO4>H2SO4 |
| B.氢化物稳定性:H2S>HF>H2O |
| C.碱性:Al(OH)3>Mg(OH)2>NaOH |
| D.氧化性:F2 > Cl2 > Br2 > I2 |
下列说法不正确的是( )
①质子数相同的微粒一定属于同一种元素②同位素的性质几乎相同③质子数相同,电子数也相同的两种微粒,不可能是一种分子和一种离子④电子数相同的微粒不一定是同一种元素⑤一种元素只能有一种质量数⑥某种元素的相对原子质量取整数,就是其质量数⑦Cl2中35Cl的原子个数之比与HCl中的35Cl与37Cl的原子个数之比相等
| A.②③⑤⑥⑦ | B.①②④⑤ |
| C.①②⑤⑥ | D.③④⑤⑥⑦ |
 、
、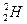 、
、 、H+、H2为( )
、H+、H2为( )
| A.氢的五种同位素 | B.五种氢元素 |
| C.氢的五种核素 | D.氢元素的五种不同微粒 |
元素X的一种同位素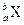 ,元素Y的一种同位素
,元素Y的一种同位素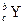 ,已知a>c,b>d,则X和Y的相对原子质量( )
,已知a>c,b>d,则X和Y的相对原子质量( )
| A.大于 | B.小于 | C.等于 | D.不能确定 |
有a、b、c、d四种元素,a、b为同周期元素,c、d为同族元素。已知a的阳离子和d的阴离子具有相同的电子层结构。b的阴离子和c的阴离子电子层结构相同。且c离子的电荷数大于b离子。则下列说法正确的是( )
①原子序数d>b>c>a②原子序数d<a<c<b③原子序数d<a<b<c④离子半径b>c>d>a⑤离子半径b>c>a>d⑥离子半径c>b>d>a
| A.③④ | B.②⑥ | C.①⑤ | D.②④ |
元素R的气态氢化物的化学式为H2R,这种气态氢化物的相对分子质量与R的最高价氧化物的相对分子质量比为1∶2.35,下列对元素R的描述正确的是( )
| A.元素R能与氧组成RO2化合物 |
| B.化合物RO2在反应中既可作氧化剂也可作还原剂,其化合物不稳定 |
| C.化合物H2R不能燃烧,也不易分解 |
| D.元素R是一种两性元素 |