下列叙述I和叙述II均正确且有因果关系的是
| 选项 |
叙述I |
叙述II |
| A |
H2有还原性,浓硫酸有强氧化性 |
不能用浓硫酸干燥H2 |
| B |
CuS难溶于水和硫酸 |
反应:H2S+CuSO4=CuS↓+H2SO4可以发生 |
| C |
海水中含有大量的Cl-、Br-等离子 |
向海水中通入F2可大量获得Cl2、Br2 |
| D |
SO2具有酸性和漂白性 |
往紫色石蕊溶液中通入SO2,溶液先变红再褪色 |
下列说法不正确的是
| A.CO2和CH4都是温室气体 |
| B.NO2和SO2都是形成酸雨的气体 |
| C.汽油和花生油的主要成分都是油酯 |
| D.毛发和蚕丝的主要成分都是蛋白质 |
短周期主族元素X、Y、Z、W原子序数依次增大。已知:X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半。下列叙述正确的是
| A.原子半径:X<W<Y<Z |
| B.X的氢化物稳定性大于Z的氢化物稳定性 |
| C.X在自然界中只能以化合态形式存在 |
| D.W的单质可使干燥的红色布条褪色 |
下列实验装置中正确的是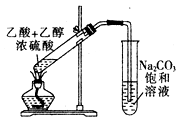
| A.实验室用液溴、苯和铁制备溴苯时必须加热 |
| B.实验室可用如右图所示装置进行酯化实验 |
| C.如果甲烷中混有少量乙烯,可以通过盛有酸性KMnO4溶液进行除杂 |
| D.将加热后的铜丝多次插入乙醇中,乙醇中可以闻到刺激性气味 |
下列叙述正确的是
| A.铜锌稀硫酸形成的原电池放电时,溶液中阳离子向铜电极移动 |
| B.燃料电池在使用时发生了燃料的燃烧 |
| C.增大反应物的用量,反应速率一定加快 |
| D.可逆反应达到一定限度后,因各物质的浓度不变,说明反应已经停止 |
为了说明影响化学反应快慢的因素,甲、乙、丙、丁4位同学分别设计了如下4个实验,你
认为结论不正确的是
| A.将形状、大小均相同的镁条和铝条与相同浓度的盐酸反应时,两者速率一样 |
| B.在相同条件下,等质量的大理石块和粉末与相同浓度的盐酸反应,大理石粉末反应快 |
| C.常温下将浓硝酸分别放在阴暗处和强光照射下,发现光照可加快浓硝酸的分解 |
| D.两只试管中分别加入相同质量的氯酸钾,其中一只试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |