设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,18g H2O含有的原子总数为3NA |
| C.标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |
| D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
下列说法正确的是
| A.在元素周期表中,每个纵列的价电子层的电子总数一定相等 |
B.在元素周期表中,s区,d区和 ds区的元素都是金属 ds区的元素都是金属 |
| C.键能是气态基态原子形成化学键释放的最低能量 |
| D.键长越长,往往键能越大,表明共价键越稳定 |
根据等电子原理,下列分子或离子与SO42-有相似结构的是
| A.PCl5 | B.CCl4 | C.NF3 | D.N |
氢键既可以存在于分子之间,也可以存在于分子内部的原子团之间,如邻羟基苯甲醛分子(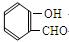 ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( HO
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( HO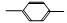 CHO )之间存在氢键(分子间氢键)。则两者的熔点、沸点的相对大小关系是
CHO )之间存在氢键(分子间氢键)。则两者的熔点、沸点的相对大小关系是
| A.前者>后者 | B.前者<后者 | C.前者=后者 | D.无法估计 |
范德华力为a KJ·mol-1,化学键为b KJ·mol-1,氢键为c KJ·mol-1,则a、b、c的大小关系是
| A.a>b>c | B.b>a>c | C.c>b>a | D.b>c>a |
下列能级中轨道数为3的是
| A.S能级 | B.P能级 | C.d能级 | D.f能级 |