如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是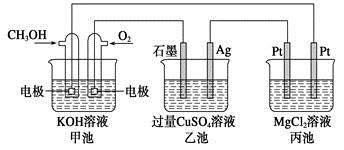
| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+ |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复原浓度 |
| D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45 g固体 |
向含溶质0.2mol的Al2(SO4)3溶液中加入1000mL KOH溶液,生成白色沉淀7.8g ,则KOH溶液的物质的量浓度可能为
| A.0.3mol/L | B.0.7mol/L | C.0.8 mol/L | D.1.5mol/L |
证明生石灰中既混有石英、又混有石灰石的正确方法是
| A.加入过量盐酸,观察是否有气泡冒出 |
| B.加入过量烧碱溶液,观察是否有固体溶解 |
| C.加热至高温、观察是否有气泡冒出,是否有硅酸钙生成 |
| D.先加过量盐酸搅拌,观察是否有不溶物剩余及气泡出现;若有不溶物则滤出,投入到氢氧化钠溶液中看其是否溶解 |
下列离子方程式书写正确的是
| A.偏铝酸钠中通足量的CO2:2AlO2— + CO2 + 3H2O = 2Al(OH)3↓ + CO32— |
| B.铜制印刷电路板:3Cu + 2Fe3+ == 3Cu2+ + 2Fe |
| C.SO2气体通入氯水中:SO2 + Cl2 + 2H2O ="=" 4H+ + Cl—+ SO42— |
| D.向水玻璃中滴加盐酸:Na2SiO3 + 2 H+ ="=" H2SiO3 ↓+ 2Na+ |
通过化合反应可以得到的物质有
| A.FeCl2 | B.FeCl3 | C.Fe2O3 | D.Al(OH)3 |
实现Al3++3A1O2—+6H2O ="=" 4Al(OH)3¯ ,正确的做法是
| A.向AlCl3溶液中不断滴入NaOH溶液 |
| B.向NaAlO2溶液中不断滴入盐酸 |
| C.向NaOH溶液中不断滴入AlCl3溶液 |
| D.向NaAlO2溶液中通入过量CO2气体 |